两个原子之间共价(covalent)和非共价债券(noncovalent bonds)的区别
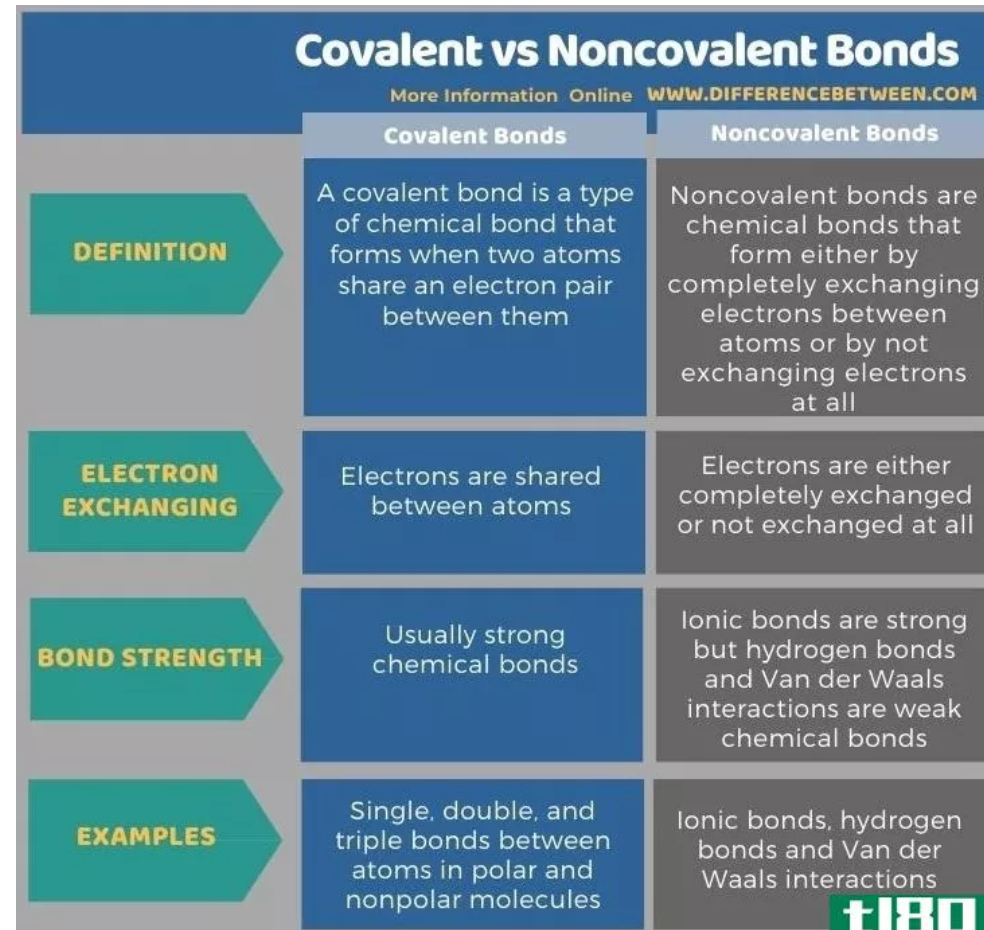
共价键和非共价键的关键区别在于,当两个原子共享它们的电子时,共价键就形成了,而非共价键则是通过两个原子之间完全交换电子或不交换任何电子而形成的。
化学键主要有四种类型:共价键、离子键、氢键和范德华相互作用。当我们把化学键分为共价键和非共价键时,离子键、氢键和范德华相互作用都属于非共价键的范畴。
什么是共价键(covalent bonds)?
共价键是两个原子共享一对电子时形成的一种化学键。它被称为“分子键”。当原子之间存在“共享对”或“键对”时,这些键就形成了。当原子共享电子时,由于原子间引力和斥力的稳定平衡而形成共价键。原子间共享电子使每个原子都有一个完整的外壳。通常,这种键形成于两个电负性值相近的非金属原子之间,或电子与带正电的金属离子之间。
共价键主要有两种类型:极性共价键和非极性共价键。极性共价键存在于两个原子之间,它们的电负性值相差在0.4到1.7之间。如果这个差值小于0.4,就会形成非极性共价键。在这里,电负性值之间的高差异意味着,一个原子(具有较高的电负性值)比另一个原子更能吸引电子,使键极性。
根据两个原子之间共享的电子对的数量,我们可以确定三种主要的共价键类型:单键,其中包括一个电子对,双键,涉及两个电子对,以及一个三键,其中包括三个电子对。
什么是非共价键(noncovalent bonds)?
非共价键是通过原子间完全交换电子或根本不交换电子而形成的化学键。非共价键有三种类型:离子键、氢键和范德华相互作用。
为了获得稳定的电子构型,原子可以获得或失去电子,并形成负电荷或正电荷粒子。我们称这些粒子为“离子”。它们之间有静电相互作用。离子键可以被描述为这些带相反电荷的离子之间的吸引力。离子间的静电相互作用受离子键中原子的电负性影响。因此,电负性可以测量原子对电子的亲和力。高电负性的原子可以从低电负性原子中吸引电子形成离子键。
氢键是另一种非共价键。它是两个不同分子的两个原子之间的一种吸引力,是一种弱吸引力。然而,与极性-极性相互作用、非极性-非极性相互作用(如范德瓦尔力)相比,氢键更强。通常,极性共价分子之间形成氢键。这些分子含有极性共价键,这种键是由于共价键中原子的电负性值不同而形成的。
范德华相互作用是另一种非共价键。它们是两个非极性分子中两个原子之间的弱引力。范德华相互作用是一种诱导吸引或排斥,它是由附近粒子的波动极化的关联引起的。
共价(covalent)和非共价债券(noncovalent bonds)的区别
共价键和非共价键是化学中两大类化学键。共价键可以在另外三个亚类中找到,如离子键、氢键和范德华相互作用。共价键和非共价键的关键区别在于,当两个原子共享它们的电子时,共价键就形成了,而非共价键则是通过两个原子之间完全交换电子或不交换任何电子而形成的。





 浙公网安备 33010602011771号
浙公网安备 33010602011771号