Cell Death Dis | 乙酰化+乳酸化修饰组联合揭示脓毒症急性肾损伤新机制

景杰生物 | 报道
急性肾损伤是脓毒症发展过程中最常见、最严重的并发症之一,发病率和死亡率高,与慢性肾脏病和终末期肾功能衰竭等不良结局有关。因此,明确脓毒症急性肾损伤 (SAKI) 发病机制对临床治疗至关重要。乳酸被认为是脓毒症预后的生物标志物,乳酸介导的非组蛋白HMGB1乳酸化修饰在脓毒症炎症反应和内皮血管通透性调控中发挥了重要作用[1]。同时有研究指出乳酸升高是脓毒症器官损伤的独立危险因素,而乳酸升高是否参与SAKI中蛋白乳酸化修饰尚不清楚。
7月21日,南方医科大学南方医院曾振华/陈仲清教授团队在国际权威学术期刊Cell Death & Disease上发表题为“”的研究论文。该研究运用多修饰组学策略(乙酰化修饰与乳酸化修饰组学)解析了丙酮酸脱氢酶 E1 亚基 α(PDHA1)的乙酰化修饰会促进乳酸含量提高,其影响下的非组蛋白Fis K20乳酸化修饰通过线粒体裂变调控SAKI的新机制。景杰生物为该研究提供了蛋白质组学、乙酰化修饰组学、乳酸化修饰组学分析技术支持以及定制抗体、乙酰化修饰、乳酸化修饰泛抗体支持。

1 肾脏线粒体蛋白乙酰化修饰组学分析
鉴于线粒体功能障碍是SAKI的重要发病机制,乙酰化修饰在调节线粒体蛋白功能中发挥关键作用。作者对Sham小鼠 (假手术组) 与盲肠结扎穿刺CLP小鼠 (脓毒症小鼠模型) 的肾脏线粒体蛋白进行乙酰化修饰组学分析,共鉴定到1042个乙酰化修饰位点,其中91个蛋白上的125个修饰位点表达水平具有显著性差异。GO富集分析表明差异修饰蛋白主要富集于细胞呼吸、三羧酸循环与氧化磷酸化代谢通路上。连接糖酵解与三羧酸循环的关键限速酶PDHA1引起了作者的注意。PDHA1有6个乙酰化修饰位点,只有K385和K267两个位点的修饰水平差异显著,K385位点又在物种间相对保守,因此作者推测PDHA1 K385乙酰化修饰可能在SAKI中发挥了重要作用。
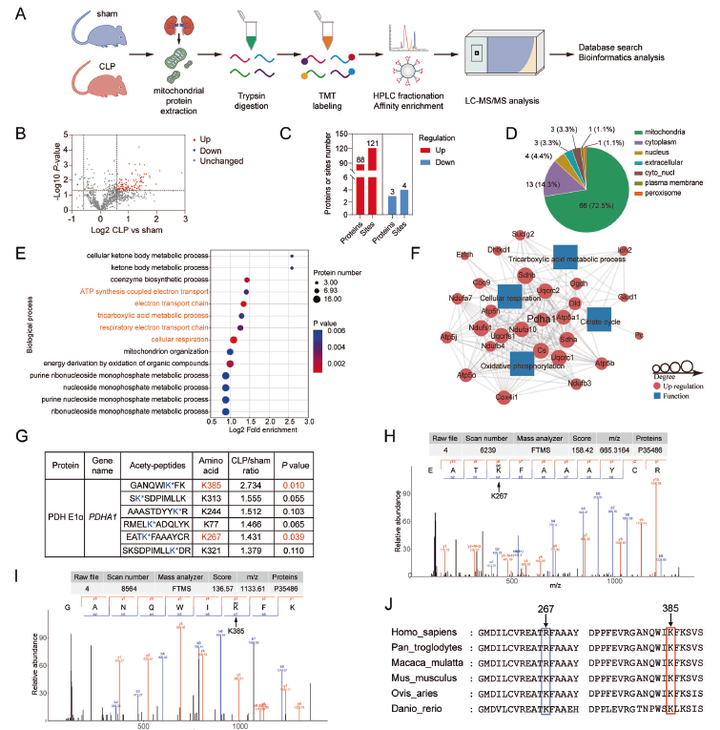
图1 肾脏线粒体蛋白乙酰化修饰组学分析
2 SIRT3下调介导了PDHA1超乙酰化并失活,导致乳酸过量累积
随后作者对乙酰化修饰组学结果进行了验证。造模24 h内,CLP小鼠肾脏中PDHA1表达无明显改变,而乙酰化修饰水平显著上升,乙酰化修饰水平上升后其活性降低。免疫荧光显示PDHA1主要在肾小管上皮细胞表达,所以后续选取肾小管上皮细胞HK-2细胞建立细胞模型。用脂多糖(LPS)刺激PDHA1 K385R点突变HK-2细胞系后,PDHA1的乙酰化水平降低,PDH活性恢复。进一步的细胞实验与动物实验表明PDHA1的乙酰化修饰是由去乙酰化酶SIRT3调控的,CLP小鼠中SIRT3表达下调,介导了PDHA1的超乙酰化与失活。最后作者探究了PDHA1失活与乳酸生成的关系,发现CLP小鼠肾乳酸水平上调。体外实验表明LPS刺激PDHA1 WT质粒转染细胞后,乳酸水平上升,PDHA1 K385R转染后减少了乳酸的生成。总之,PDHA1的高乙酰化和失活促进了乳酸的累积,MIMIC-IV 数据库表明乳酸升高与临床脓毒症患者的SAKI发病率高和预后不良有关,实验表明乳酸处理小鼠后可通过介导肾小管上皮细胞损伤加重SAKI。
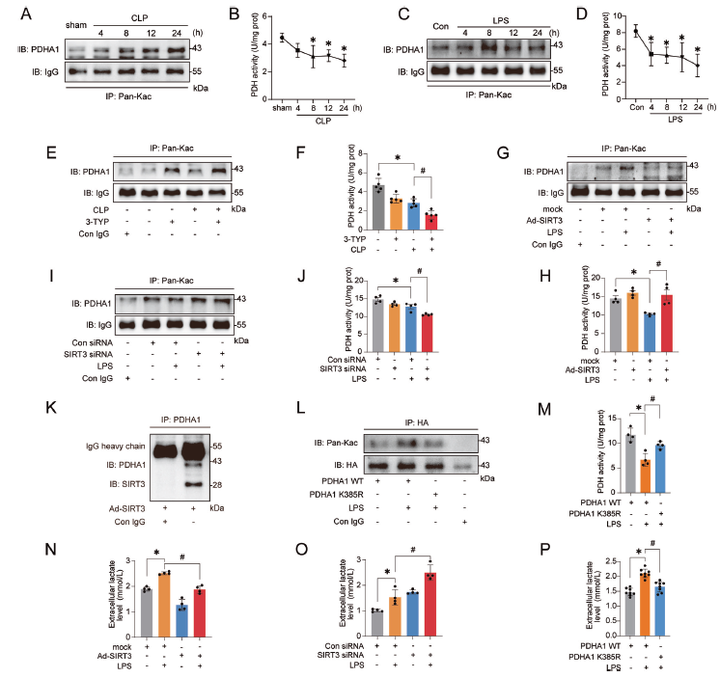
图2 SIRT3下调介导了PDHA1超乙酰化和失活,导致乳酸过量生成
3 肾脏乳酸化修饰组学检测
鉴于乳酸在SAKI中发挥重要作用,且乳酸可介导蛋白质赖氨酸残基发生乳酸化修饰,进而调控多种生物学过程。因此作者首先利用乳酸化修饰泛抗体进行了整体乳酸化水平的检测,发现与Sham小鼠相比,CLP小鼠肾脏中的乳酸化水平明显改变,说明乳酸化修饰确实参与了SAKI发展。随后,作者对两组小鼠肾脏进行了基于4D-label free的乳酸化修饰组学检测,分析显示50%差异修饰蛋白定位于线粒体中,功能富集分析表明差异修饰蛋白参与线粒体结构的调节。作者关注到了线粒体裂变1蛋白 (Fis1),一种线粒体网络调节因子,同时是乳酸化水平上调最显著的蛋白。随后作者对组学结果进行了表达验证。IP结果表明,CLP后小鼠肾脏Fis1乳酸化水平显著升高,乳酸给药后Fis1乳酸化水平进一步上调。同时体外实验表明,乳酸和LPS刺激显著上调了HK-2细胞的Fis1乳酸化水平。这些结果表明,Fis1乳酸化修饰可能在SAKI中起重要作用。
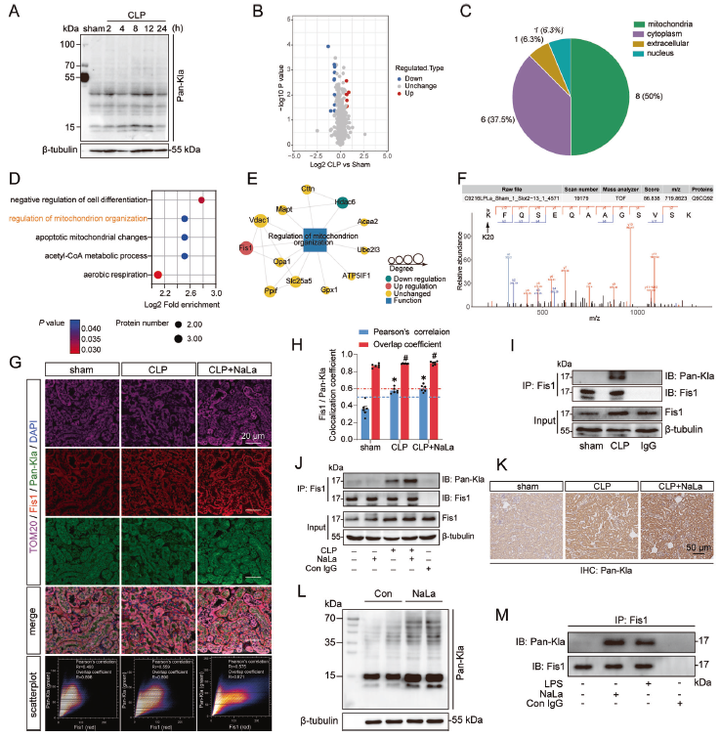
图3 乳酸化修饰组学分析显示脓毒症后肾脏Fis1乳酸化修饰水平上升
4 Fis1 K20乳酸化修饰在SAKI中发挥关键作用
乳酸化修饰组学分析发现K20为Fis1乳酸化修饰位点。Fis1是一种线粒体外膜衔接蛋白,可以与动力蛋白相关蛋白1 (DRP1) 相互作用介导线粒体裂变。为了检测Fis1 K20乳酸化修饰是否能够调控线粒体裂变,作者定制了Fis1 K20乳酸化修饰位点特异性抗体,该抗体可以特异性识别Fis1 K20乳酸化修饰肽段。随后作者构建了Fis1 K20 WT以及Fis1 K20R点突变HK-2细胞系,发现Fis1 K20乳酸化修饰显著促进了细胞线粒体裂变,进而促进线粒体活性氧mtROS生成、介导ATP耗竭、并加重细胞凋亡。另外,作者对细胞进行二氯乙酸钠 (DCA,(PDHA1激活剂) 处理及诱导细胞SIRT3过表达,结果显示两种处理均降低了Fis1 K20乳酸化水平,进而缓解了LPS诱导的细胞活力和ATP水平的降低。对CLP小鼠腹腔注射DCA后改善了肾脏病理损伤,GSK治疗 (乳酸脱氢酶抑制剂以减少乳酸产生) 同样遏制了3-TYP (SIRT3抑制剂) 介导的SAKI加重。这些实验结果表明,减少乳酸生成和Fis1乳酸化修饰可以改善肾小管上皮细胞损伤并减轻SAKI。
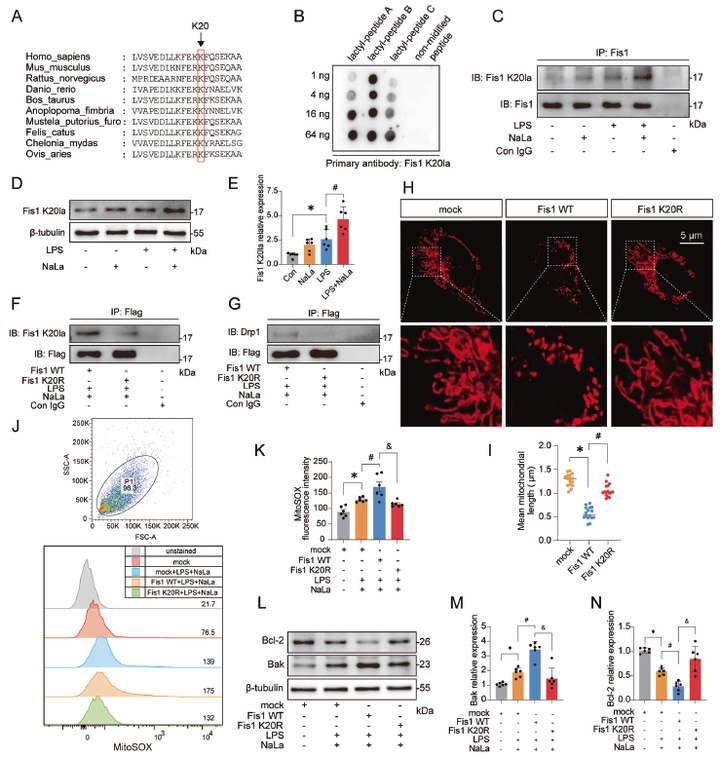
图4 Fis1 K20乳酸化修饰在SAKI中发挥关键作用
综上所述,该研究通过乙酰化修饰组学以及乳酸化修饰组学检测揭示了乳酸与脓毒症器官损伤联系的新机制。研究表明SAKI小鼠肾脏中SIRT3表达下调,导致PDHA1超乙酰化和失活,进而促进肾小管上皮细胞中乳酸的累积。乳酸的累积进一步介导了Fis K20的乳酸化修饰,最后促进线粒体过度裂变,加重细胞凋亡。降低Fis1 K20乳酸化修饰能够改善肾小管上皮细胞损伤并减轻SAKI,为SAKI的新型治疗策略提供了研究思路。
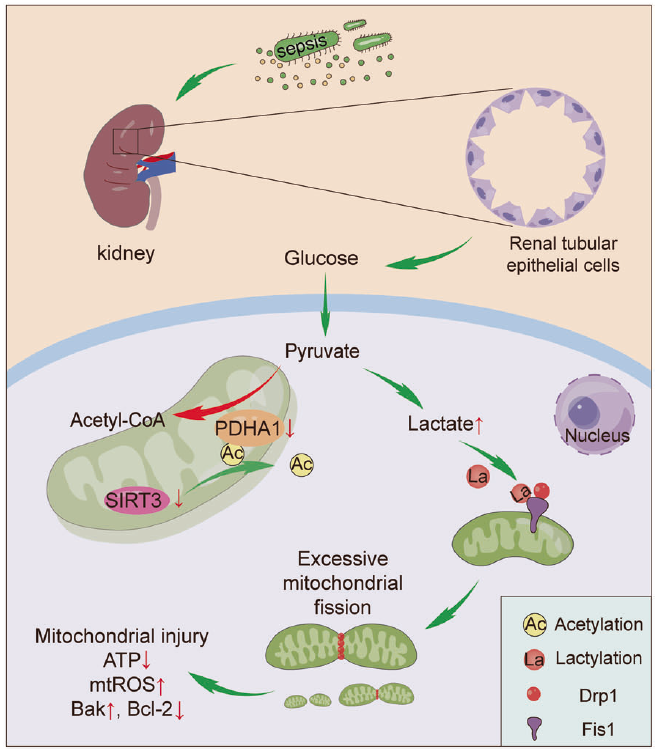
图5 研究机制示意图
本研究给我们也提供了机制研究的新思路,即:此前的很多研究均是在蛋白角度解释多个蛋白相互作用最终形成功能通路影响表型,或者是通过单一修饰组学研究某蛋白的修饰对于通路的影响。而在实际生物学现象中,某个功能通路不只是受某一修饰影响,而是多种翻译后修饰的交叉有序调控下行使作用的,这也就提示了我们以多修饰组学研究高精度解析生物学现象机制的重要意义。
参考文献
1. Yang K, . 2022. Lactate promotes macrophage HMGB1 lactylation, acetylation, and exosomal release in polymicrobial sepsis. .
2. Sheng An, . 2023. PDHA1 hyperacetylation-mediated lactate overproduction promotes sepsis-induced acute kidney injury via Fis1 lactylation. .
景杰生物作为修饰组学领域的领跑者,拥有多种修饰抗体和修饰组学质谱检测服务。如果您想了解相关产品和服务的更多信息,请扫描下方二维码填写合作咨询表单、或咨询景杰生物销售工程师、或拨打科服热线400-100-1145。如有转载、投稿等其他合作需求,请在文章下方留言,或添加微信ptm-market咨询。


 浙公网安备 33010602011771号
浙公网安备 33010602011771号