Cell Rep | 任文凯/印遇龙院士团队琥珀酰化修饰组学揭示GABA调控巨噬细胞命运机制

神经系统和免疫系统常被单独研究,但越来越多的证据显示,神经元、神经肽以及神经递质可以影响免疫细胞命运。γ-氨基丁酸 (GABA) 能系统是中枢神经系统的重要组成部分,由GABA,GABA受体,谷氨酸脱羧酶,囊泡抑制氨基酸转运体,GABA转运体和转氨酶组成。免疫细胞具有谷氨酸脱羧酶,GABA受体和转运体,并且能够生成GABA,说明GABA能系统在免疫细胞激活和功能上可能具有重要的作用。尽管关于GABA信号通路在T细胞命运决定作用的研究越来越多,而氨基酸GABA代谢能否以及如何塑造固有免疫细胞 (如巨噬细胞) 的功能至今仍不明确。
近期,华南农业大学任文凯教授/湖南农业大学印遇龙院士研究团队在国际知名学术期刊Cell Reports (IF=9.995) 上发表了题为 GABA regulates IL-1β production in macrophages 的研究性论文。该研究发现了GABA在巨噬细胞命运调控中的重要作用,证明了GABA通过增强FAD (黄素腺嘌呤二核苷酸) -LSD1 (赖氨酸特异性去甲基酶1) 信号以调节Bcl2l11和Dusp2基因结合组蛋白的去甲基化,进而降低了炎性小体复合体形成的作用机制,GABA还能降低线粒体蛋白的琥珀酰化修饰,进而促进氧化磷酸化 (OXPHOS) 。此外GABA可以缓解脂多糖 (LPS) 诱导的脓毒症模型和高脂饮食诱导的肥胖小鼠表型,为治疗巨噬细胞相关的炎症疾病提供了新的策略。景杰生物为该研究提供了琥珀酰化修饰组学服务和乙酰化、琥珀酰化、丙二酰化、乳酸化修饰泛抗体产品。

01 GABA限制巨噬细胞IL-1β的生成
作者首先分析了在GABA处理后的M1巨噬细胞IL-1β的分泌情况。结果发现,GABA无法调节M1巨噬细胞的IL-1β的分泌,且对极化过程中的巨噬细胞同样没有作用。鉴于巨噬细胞从单核细胞分化而来,作者在小鼠体内进行实验,在巨噬细胞的成熟过程中腹腔注射GABA。结果表明,GABA可以有效地抑制M1巨噬细胞IL-1β的表达和生成。为验证这一发现,作者在单核细胞系J774a.1和骨髓来源巨噬细胞BMDM的成熟过程中进行了相似的处理,发现IL-1β的生成得到有效的抑制,说明GABA可以影响巨噬细胞的成熟。通过对IL-1β生成的相关通路 (NF-kB、炎症小体以及mTOR等) 进行分析,GABA处理可以有效的抑制巨噬细胞M1的炎症信号的激活。此外,鉴于线粒体功能同样会对IL-1β的生成发挥重要作用,研究通过对线粒体面积、氧气消耗速率、线粒体融合等进行了细致的分析,证实了GABA的处理可以增强巨噬细胞线粒体的功能。综上,GABA通过抑制成熟过程中巨噬细胞的炎症信号和增强线粒体功能介导IL-1β的下调。
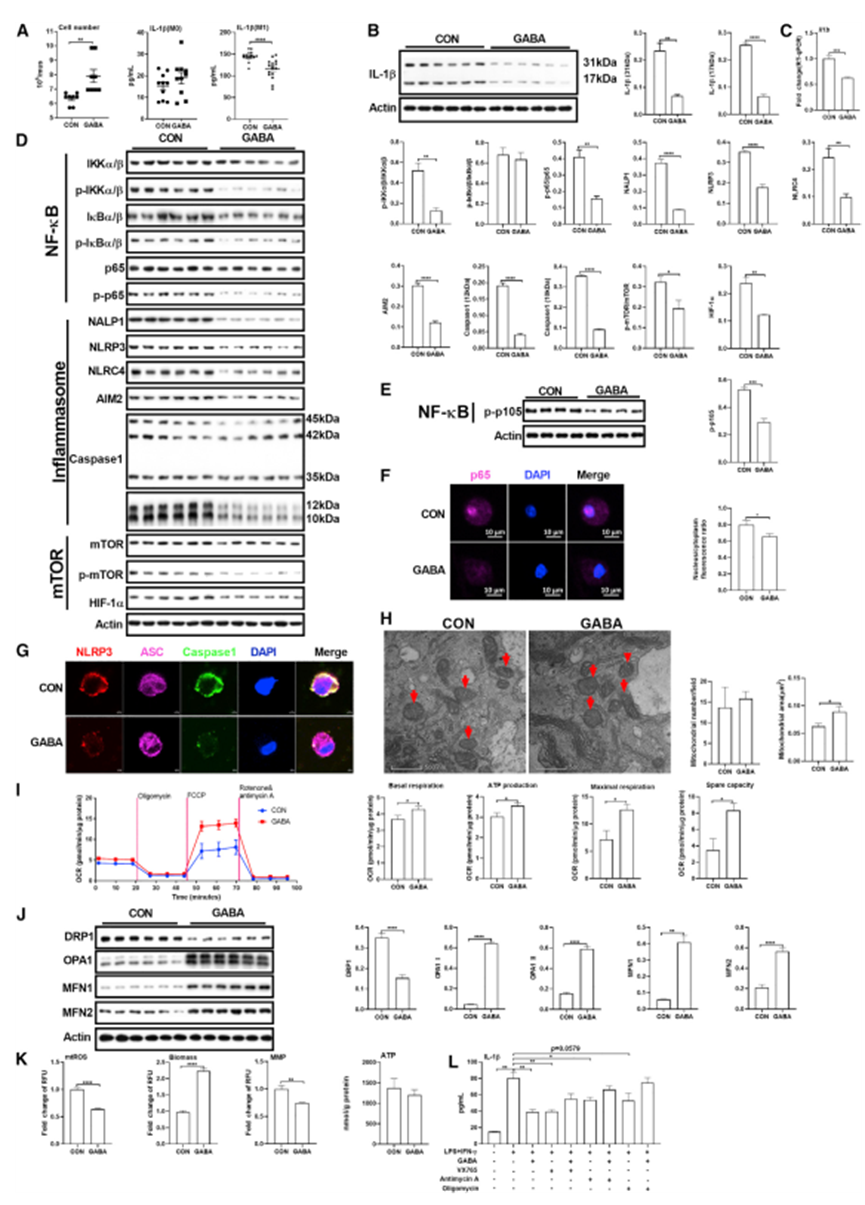
图1 GABA限制巨噬细胞IL-1β的生成
02 GABA通过调节线粒体蛋白的琥珀酰化修饰增强氧化磷酸化过程
参与线粒体代谢的酶的活性广泛受到翻译后修饰的调控,如乙酰化、乳酸化、丙二酰化和巴豆酰化。通过对M1巨噬细胞进行不同修饰水平分析,研究发现仅有琥珀酰化修饰表现出明显的变化。而鉴于琥珀酰辅酶A (SCOA) 由α-酮戊二酸通过羟戊二酸脱氢酶 (OGDH) 转化而来,而且GABA又能转化成琥珀酸并拮抗OGDH活性。作者进一步分析了GABA处理后M1巨噬细胞的SCOA含量和OGDH活性,并发现GABA的处理会下调M1巨噬细胞的SCOA含量并且抑制OGDH活性。因此,GABA可以通过下调SCOA水平影响琥珀酰化修饰过程,进而增强线粒体功能。通过基于高分辨质谱的琥珀酰化修饰组学分析,研究发现GABA处理的M1巨噬细胞的琥珀酰化修饰的蛋白数和修饰位点均出现了显著的下降,且这些差异蛋白大部分分布于线粒体当中。GO和KEGG富集分析结果表明,在GABA处理后的M1巨噬细胞中,参与糖酵解、三羧酸循环以及OXPHOS的代谢酶的琥珀酰化修饰出现了显著下调。因此,GABA通过降低线粒体蛋白的琥珀酰化修饰以增强线粒体功能。
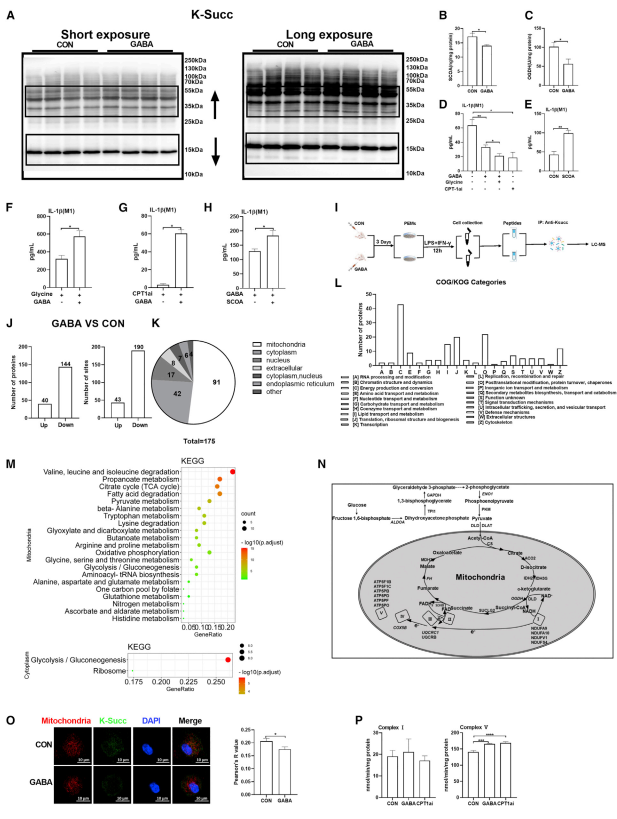
图2 GABA通过降低线粒体蛋白琥珀酰化修饰增强线粒体功能
03 GABA增强FAD-LSD1信号通路调节BCL2L11和DUSP2的表达
细胞代谢与巨噬细胞功能联系紧密。作者发现,GABA的处理会增强线粒体功能,进而显著地影响M0和M1巨噬细胞的胞内代谢,如FAD、磷酰胆碱、组胺和谷氨酸增加,而L-谷氨酰胺出现下降。对细胞进行FAD处理,结果表明FAD能像GABA一样抑制炎症信号的激活和增强线粒体功能,进而抑制巨噬细胞IL-1β的生成。因此GABA是通过FAD影响巨噬细胞IL-1β的生成。
以前的研究表明,巨噬细胞的极化是代谢和表观遗传的共同结果。FAD是LSD1一种重要的辅因子,而LSD1会通过作用H3K4me1/2和H3K9me1/2调节基因表达。通过对巨噬细胞的GABA处理,研究发现LSD1的蛋白丰度会有提升并伴有H3K4me1,H3K4me2,H3K9me1以及H3K9me2水平的降低。通过使用LSD1的抑制剂进行处理后,GABA介导的IL-1β和炎性小体表达的下调会被完全逆转。因此,GABA通过FAD-LSD1的激活限制M1巨噬细胞的IL-1β的生成。
为进一步探究其背后的分子机制,作者对经过不同处理的细胞进行转录组分析。结果表明,GABA或FAD处理后的差异表达基因富集于胞内代谢和信号通路中 (NF-kB,炎症小体以及mTOR) 。为了确定影响GABA介导的IL-1β表达的关键差异基因,作者对组学数据进行了筛选,并选择了BCL2L11和DUSP2进行后续的研究。BCL2L11和DUSP2的沉默可以有效地逆转GABA介导的IL-1β的调控作用。由于LSD1行使去甲基功能,通过结合ChIP-qPCR实验,实验结果表明BCL2L11和DUSP2的表达增加极有可能是H3K4/9me2的去甲基化所导致的,而LSD1抑制剂处理对IL-1β的调控作用会被BCL2L11和DUSP2的过表达所屏蔽。所以,GABA通过LSD1上调BCL2L11和DUSP2的表达,进而限制M1巨噬细胞IL-1β的生成。
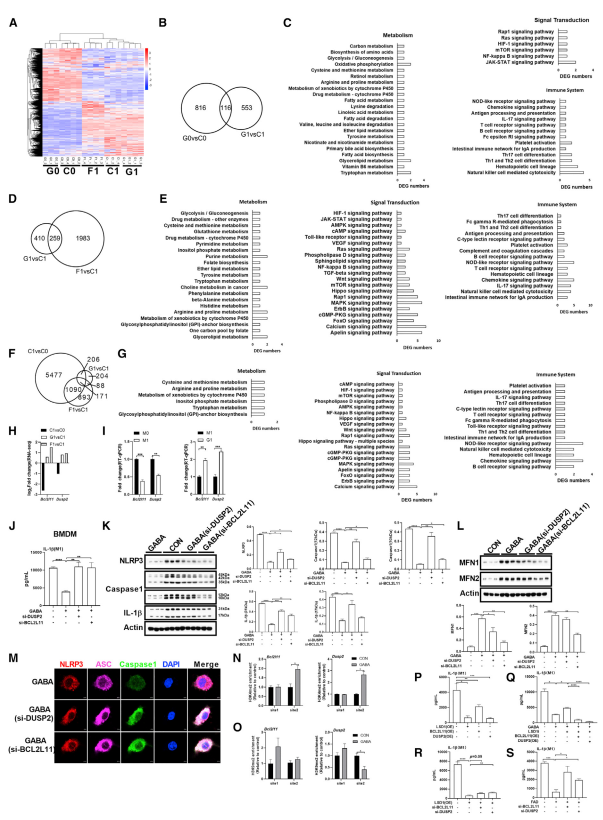
图3 LSD1通过Bcl2l11和Dusp2减轻巨噬细胞IL-1β的生成
04 GABA减轻小鼠的体内炎症反应
最后,作者探究GABA在体内是否可以抑制炎症反应。在第一个LPS诱导的脓毒症模型 (急性炎症) 中,口服GABA的小鼠表现出更高的生存率,且血清和肺部的炎症细胞因子的分泌出现了显著的下降,肺部损伤也出现了明显改善。在第二个由高脂饮食诱导的慢性炎症模型中,尽管GABA的治疗对小鼠体重的影响较小,但是GABA治疗组中小鼠的内脏脂肪的重量下降,并有效的预防血糖和胰岛素的耐受。综上,GABA在体内能有效地缓解巨噬细胞介导的急性和慢性炎症。
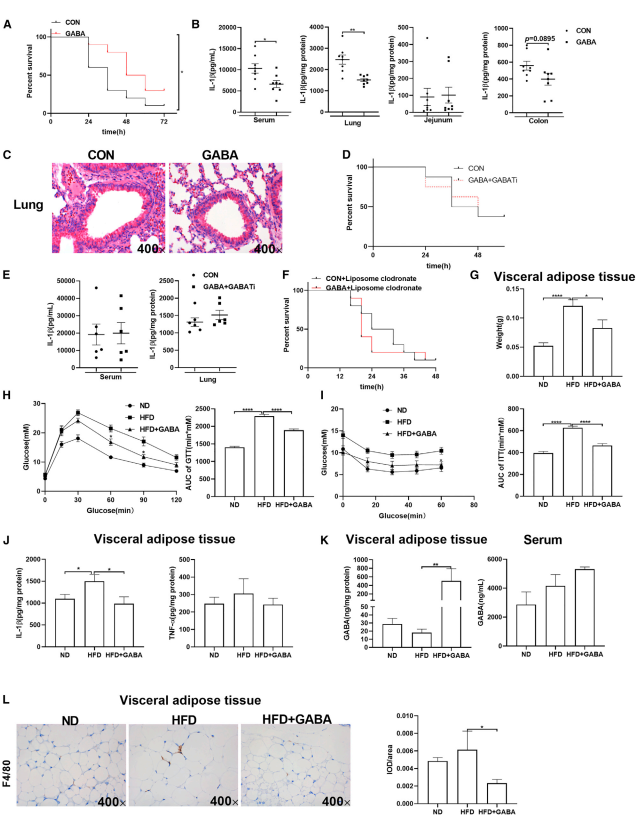
图4 GABA在体内可以减轻巨噬细胞介导的急性和慢性炎症
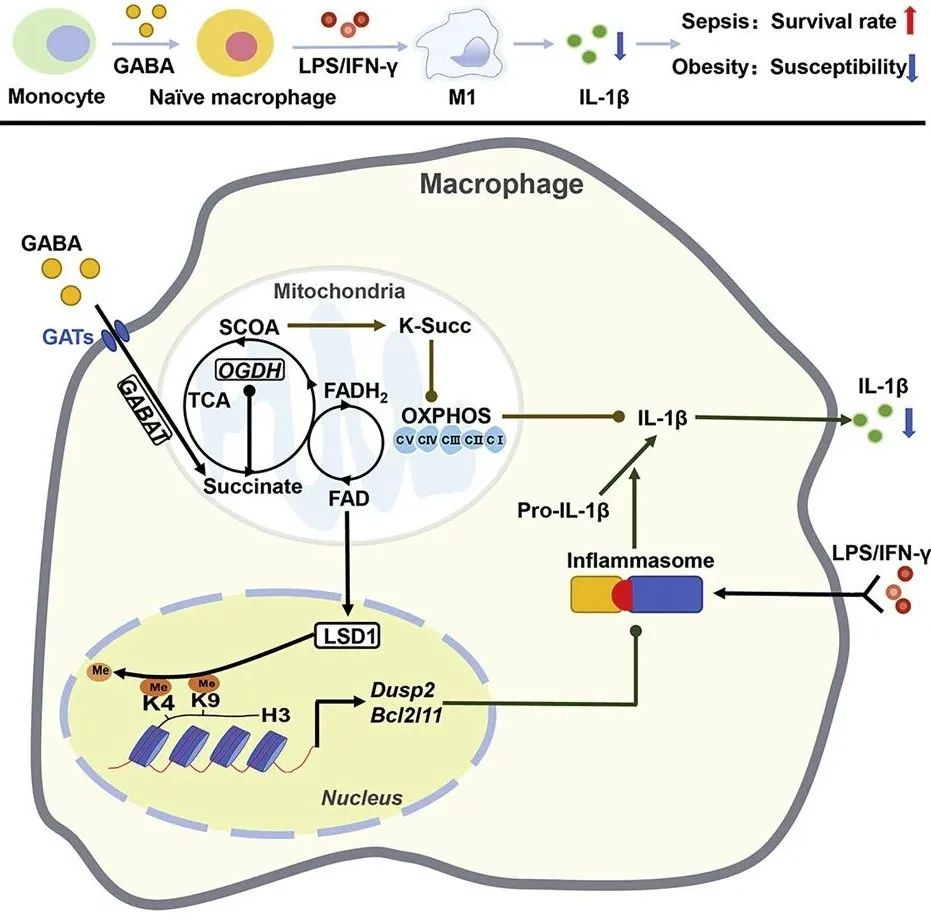
综上所述,该文章证明了GABA可以调节巨噬细胞成熟和炎症反应。一方面GABA可以通过FAD-LSD1信号通过表观遗传抑制炎症小体的生成,同时也通过琥珀酰化修饰抗体和琥珀酰化修饰组学证明了GABA通过下调线粒体蛋白的琥珀酰化修饰,进而增强线粒体功能的关键机制。鉴于神经递质的广泛存在和巨噬细胞在体内免疫过程中的重要作用,该工作为神经递质决定免疫细胞命运的科学研究和相应的治疗方法开发奠定了坚实的理论基础。
参考文献
1. Jian Fu, et al. 2022. GABA regulates IL-1β production in macrophages. Cell Reports.
本文由景杰学术团队报道,欢迎转发到朋友圈。如有转载、投稿等其他合作需求,请文章下方留言,或添加微信ptm-market咨询。


 浙公网安备 33010602011771号
浙公网安备 33010602011771号