尼帕病毒(Nipah virus)是什么?从RNA结构到实验室研究技术详解
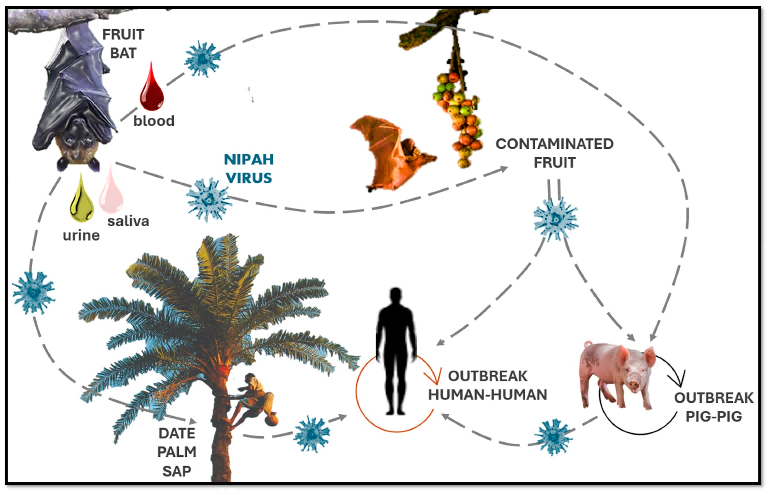
尼帕病毒(Nipah virus,NiV)是亨德拉尼帕病毒属的一种高致病性人畜共患病原体,其自然宿主为狐蝠科果蝠。自1999年在马来西亚首次暴发以来,该病毒因其高致死率(40%-75%)和引发脑炎、严重呼吸道疾病的特性,被世界卫生组织列为优先研究的病原体之一。理解其独特的单股负链RNA基因组结构和复制机制,是开发有效研究工具和防控策略的基础。本文将从病毒基因组RNA的基本结构入手,系统阐述其实验室研究中所涉及的核心技术与方法,为相关领域的科研人员提供全面的技术视角。
一、尼帕病毒的RNA基因组结构与复制机制
尼帕病毒的遗传物质是一条单股负链RNA(-ssRNA),基因组全长约为18.2kb。与正链RNA病毒不同,其基因组RNA本身不具备感染性,必须与病毒自身编码的RNA依赖的RNA聚合酶(RdRp)结合形成核糖核蛋白复合体(RNP),才能启动复制与转录。
基因组组织特征:
NiV的基因顺序高度保守,从3‘端到5’端依次为:先导序列(leader)-N-P-M-F-G-L-尾随序列(trailer)。这些基因之间由非编码的基因间隔区隔开,其中包含转录终止、重新起始和多聚腺苷酸化信号。这种“一个启动,一个终结”的转录模式,使得下游基因的转录效率逐级递减,从而精细调控各病毒蛋白的表达水平。
P基因的复杂性:
磷蛋白(P)基因是基因组复杂性的集中体现。通过一种独特的RNA编辑机制(在特定位点插入非模板化的G核苷酸),P基因的mRNA可被翻译成四种不同的蛋白质:P蛋白本身,以及非结构蛋白V、W和C。这些蛋白,尤其是V和W,是病毒对抗宿主I型干扰素(IFN-α/β) 先天免疫应答的关键武器。
复制与转录循环:
病毒进入细胞后,RNP核心释放到细胞质中。病毒编码的L蛋白(大聚合酶蛋白) 与P蛋白组成的复合物,首先以基因组负链RNA为模板,合成正链的反基因组RNA(antigenomicRNA),此过程为复制。同时,聚合酶复合物也从基因组模板上合成6条独立的、带帽并多聚腺苷酸化的单顺反子mRNA,此过程为转录。新合成的mRNA被宿主核糖体翻译成病毒蛋白,而新合成的反基因组RNA则作为模板,大量产生子代病毒的基因组RNA。
二、实验室研究核心技术详解
基于对NiVRNA基因组和病毒蛋白功能的认知,一系列标准化的实验室研究技术被建立起来,这些技术是深入探索病毒生物学、宿主互作及评估抗病毒策略的基础。
病毒培养与分离技术:
生物安全要求:所有涉及活NiV的操作必须在生物安全四级(BSL-4) 实验室或具备等效防护条件的设施中进行,这是首要前提。
细胞培养系统:NiV能在多种细胞系中良好复制,常用的包括VeroE6(非洲绿猴肾细胞)、BHK-21(幼仓鼠肾细胞)和HEK293T(人胚肾细胞)等。VeroE6细胞因缺乏I型干扰素应答,常被用于高效分离和扩增病毒。
病毒滴定:采用空斑形成试验(PlaqueAssay)或终点稀释法(如TCID50)来定量病毒滴度。空斑试验需要在细胞单层上覆盖琼脂糖或羧甲基纤维素以限制病毒扩散,形成肉眼可见的空斑。
基于RNA的分子检测技术:
逆转录-聚合酶链式反应(RT-PCR)与实时荧光定量RT-PCR(qRT-PCR):这是诊断和研究中检测病毒RNA最灵敏、最常用的方法。针对高度保守的N基因或L基因区域设计特异性引物和探针,可从临床样本(如脑脊液、咽拭子)或细胞培养上清中快速检测到病毒核酸。qRT-PCR还能实现对病毒载量的精确定量。
血清学检测技术:
酶联免疫吸附试验(ELISA):用于检测宿主针对NiV产生的特异性抗体(IgG和IgM)。通常使用重组表达的病毒核衣壳蛋白(N)或糖蛋白(G)作为包被抗原。N蛋白免疫原性强,常用于筛查;而针对G蛋白的抗体的检测更具特异性,可用于确诊和中和抗体评估。
血清中和试验:这是评估抗体中和活性的“金标准”。在BSL-4实验室中,将连续稀释的血清样本与固定量的活病毒混合,接种到易感细胞中,通过观察细胞病变效应(CPE)或采用免疫荧光法检测,计算能保护50%细胞免受感染的血清稀释度,即中和效价(NT50)。为降低生物安全风险,现已开发出基于假病毒颗粒(PseudotypedVirus)的中和试验。
蛋白结构与功能研究技术:
重组蛋白表达与应用:利用原核(如大肠杆菌)或真核(如昆虫杆状病毒系统、哺乳动物HEK293/CHO细胞)表达系统,大量生产高纯度的NiV关键蛋白(如F、G蛋白的胞外域、N蛋白等)。这些重组蛋白是研究蛋白-蛋白相互作用(如G蛋白与Ephrin-B2/B3受体结合)、表位作图、开发诊断试剂和筛选抑制剂的宝贵工具。
假病毒系统:这是在不操作活病毒的情况下,研究病毒进入机制的强大工具。将NiV的F和G蛋白表达质粒与携带报告基因(如荧光素酶、绿色荧光蛋白)的病毒核心骨架质粒共转染细胞,可组装出仅能完成单轮感染、不产生复制性后代的假病毒。该系统广泛用于评估中和抗体活性、研究受体使用以及筛选进入抑制剂,极大降低了研究门槛和风险。
反向遗传学技术:
这是目前研究NiV生命周期的顶尖工具。通过构建包含全长NiVcDNA克隆的质粒,在辅助质粒提供病毒N、P、L蛋白的情况下,在细胞内转录和组装出具有感染性的病毒RNP,从而拯救出活病毒。这项技术允许研究人员在DNA水平上对病毒基因组进行精确的定点突变、基因敲除或插入报告基因,从而在分子水平上剖析特定基因或非编码序列在病毒复制、致病和免疫逃逸中的具体功能。


 浙公网安备 33010602011771号
浙公网安备 33010602011771号