化学笔记:粗盐提纯
粗盐提纯
powered by Typora
——hsy8116
产率误差分析
| 步骤 | 错误操作 | 误差 | 原因 |
|---|---|---|---|
| 溶解 | 粗盐未完全溶解 | 偏小 | 未溶解的粗盐在下一步被当成滤渣除去 |
| 过滤 | 滤纸破损 | 偏大 | 粗盐中固体杂质混入滤液 |
| 过滤 | 未引流 | 偏小 | 含有氯化钠的液体飞溅 |
| 过滤 | 液面高于滤纸 | 偏大 | 粗盐中固体杂质混入滤液 |
| 过滤 | 未洗涤 | 偏小 | 含有氯化钠的液体残留在玻璃棒、滤纸、漏斗中 |
| 蒸发 | 未搅拌 | 偏小 | 局部温度过高,含有氯化钠的液体飞溅 |
| 蒸发 | 一有固体析出就停止加热 | 偏大 | 氯化钠固体中混有少量水 |
| 蒸发 | 全部蒸干时停止加热 | 偏小 | 氯化钠固体飞溅 |
注:
偏小 \(\rarr\) 损失 \(\rm NaCl\)
偏大 \(\rarr\) 杂质当产率(难溶性杂质或水)
玻璃棒的作用
-
溶解:搅拌,加快粗盐的溶解
-
过滤:引流,防止液体飞溅
-
蒸发:搅拌,防止液体局部温度过高,造成液体飞溅
-
转移:转移固体
除去粗盐中可溶性杂质
\(\rm NaCl(CaCl_2)\)
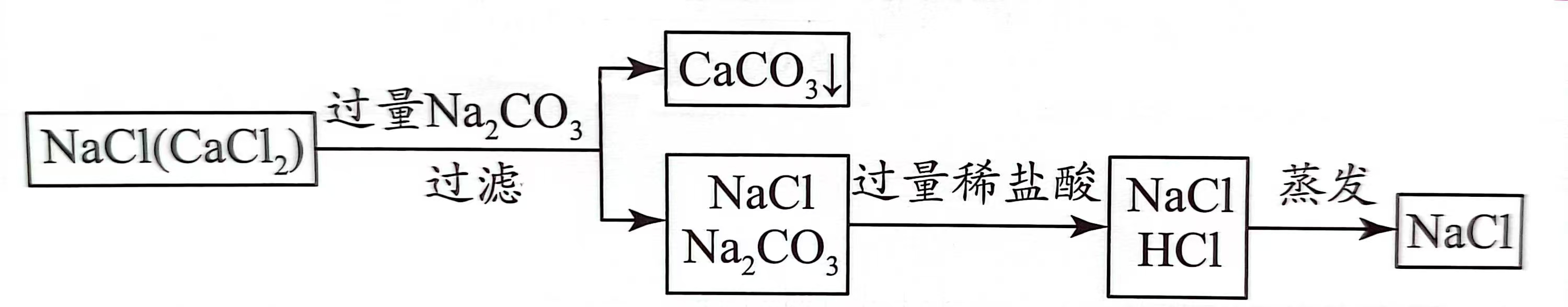
-
\(\rm CaCl_2(杂质) \xrightarrow{转化} NaCl\):① \(\rm Ca^{2+}\) 反应 ② 添加 \(\rm Na^+\)
\(\boxed{\rm Na_2CO_3 + CaCl_2 \xlongequal{\ \ \ \ } CaCO_3 \darr + 2NaCl}\)
-
\(\rm Na_2CO_3 (新杂质) \xrightarrow{转化} NaCl\):① \(\rm CO_3^{2-}\) 反应 ② 添加 \(\rm Na^+\)
\(\boxed{\rm Na_2CO_3 + 2HCl \xlongequal{\ \ \ \ } 2NaCl + H_2O + CO_2 \uarr}\)
-
蒸发:① \(\rm H_2O\) ② \(\rm HCl气体(新杂质)\)
\(\rm NaCl(MgCl_2)\)
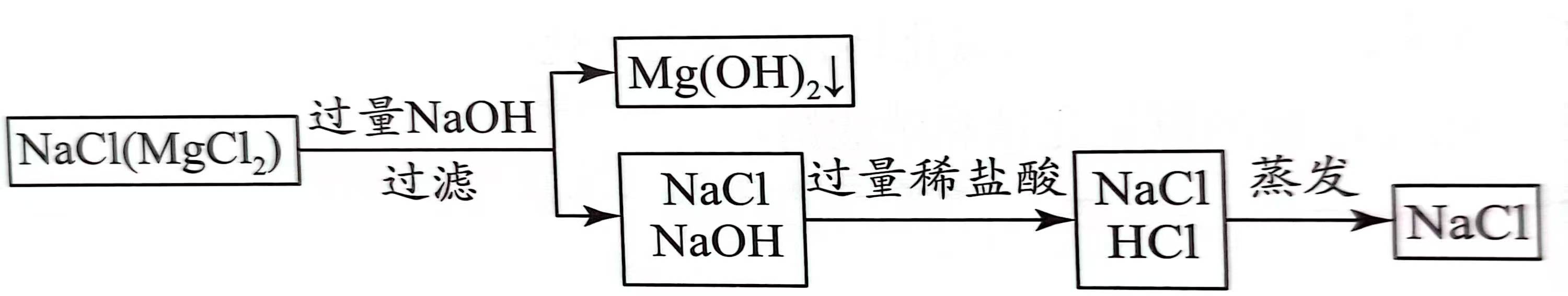
-
\(\rm MgCl_2(杂质) \xrightarrow{转化} NaCl\):① \(\rm Mg^{2+}\) 反应 ② 添加 \(\rm Na^+\)
\(\boxed{\rm 2NaOH + MgCl_2 \xlongequal{\ \ \ \ } Mg(OH)_2 \darr + 2NaCl}\)
-
\(\rm NaOH (新杂质) \xrightarrow{转化} NaCl\):① \(\rm OH^-\) 反应 ② 添加 \(\rm Cl^-\)
\(\boxed{\rm NaOH + HCl \xlongequal{\ \ \ \ } NaCl + H_2O}\)
-
蒸发:① \(\rm H_2O\) ② \(\rm HCl气体(新杂质)\)
\(\rm NaCl(Na_2SO_4)\)
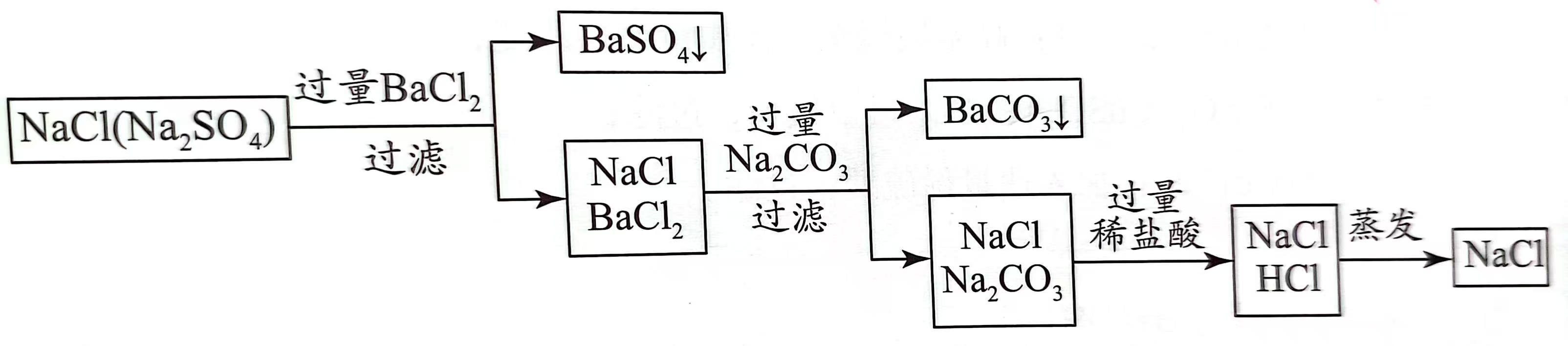
-
\(\rm Na_2SO_4(杂质) \xrightarrow{转化} NaCl\):① \(\rm SO_4^{2-}\) 反应 ② 添加 \(\rm Cl^-\)
\(\boxed{\rm Na_2SO_4 + BaCl_2 \xlongequal{\ \ \ \ } BaSO_4 \darr + 2NaCl}\)
-
\(\rm BaCl_2 (新杂质) \xrightarrow{转化} NaCl\):① \(\rm Ba^{2+}\) 反应 ② 添加 \(\rm Na^+\)
\(\boxed{\rm Na_2CO_3 + BaCl_2 \xlongequal{\ \ \ \ } BaCO_3 \darr + 2NaCl}\)
-
\(\rm Na_2CO_3 (新杂质) \xrightarrow{转化} NaCl\):① \(\rm CO_3^{2-}\) 反应 ② 添加 \(\rm Na^+\)
\(\boxed{\rm Na_2CO_3 + 2HCl \xlongequal{\ \ \ \ } 2NaCl + H_2O + CO_2 \uarr}\)
-
蒸发:① \(\rm H_2O\) ② \(\rm HCl气体(新杂质)\)
多种杂质共同除去 + 优化
-
过量 \(\rm BaCl_2\) \(\xrightarrow{\rm 除去 Na_2SO_4}\) 过量 \(\rm Na_2CO_3\) \(\xrightarrow{\rm 除去 CaCl_2, BaCl_2}\) 过量 \(\rm NaOH\) \(\xrightarrow{\rm 除去 MgCl_2}\) 过滤 \(\xrightarrow{}\) 过量稀盐酸 \(\xrightarrow{\rm 除去 NaOH, Na_2CO_3}\) 蒸发结晶
杂质 \ 除杂剂(操作) 溶解 \(\rm CaCl_2\) \(\rm MgCl_2\) \(\rm Na_2SO_4\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm CaCl_2\) \(\rm MgCl_2\) \(\xcancel{\rm Na_2SO_4}\) \(\rm BaSO_4 \darr\) \(\rm BaCl_2\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm Na_2CO_3\) \(\xcancel{\rm CaCl_2}\) \(\rm CaCO_3 \darr\) \(\rm MgCl_2\) \(\xcancel{\rm Na_2SO_4}\) \(\rm BaSO_4 \darr\) \(\xcancel{\rm BaCl_2}\) \(\rm BaCO_3 \darr\) \(\rm Na_2CO_3\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm Na_2CO_3\) \(\rm NaOH\) \(\xcancel{\rm CaCl_2}\) \(\rm CaCO_3 \darr\) \(\xcancel{\rm MgCl_2}\) \(\rm Mg(OH)_2 \darr\) \(\xcancel{\rm Na_2SO_4}\) \(\rm BaSO_4 \darr\) \(\xcancel{\rm BaCl_2}\) \(\rm BaCO_3 \darr\) \(\rm Na_2CO_3\) \(\rm NaOH\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm Na_2CO_3\) \(\rm NaOH\) 过滤 \(\xcancel{\rm CaCl_2}\) \(\xcancel{\rm CaCO_3 \darr}\) \(\xcancel{\rm MgCl_2}\) \(\xcancel{\rm Mg(OH)_2 \darr}\) \(\xcancel{\rm Na_2SO_4}\) \(\xcancel{\rm BaSO_4 \darr}\) \(\xcancel{\rm BaCl_2}\) \(\xcancel{\rm BaCO_3 \darr}\) \(\rm Na_2CO_3\) \(\rm NaOH\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm Na_2CO_3\) \(\rm NaOH\) 过滤 \(\rm HCl\) \(\xcancel{\rm CaCl_2}\) \(\xcancel{\rm CaCO_3 \darr}\) \(\xcancel{\rm MgCl_2}\) \(\xcancel{\rm Mg(OH)_2 \darr}\) \(\xcancel{\rm Na_2SO_4}\) \(\xcancel{\rm BaSO_4 \darr}\) \(\xcancel{\rm BaCl_2}\) \(\xcancel{\rm BaCO_3 \darr}\) \(\xcancel{\rm Na_2CO_3}\) \(\rm H_2O+ CO_2 \uarr\) \(\xcancel{\rm NaOH}\) \(\rm H_2O\) \(\rm HCl\) 杂质 \ 除杂剂(操作) 溶解 \(\rm BaCl_2\) \(\rm Na_2CO_3\) \(\rm NaOH\) 过滤 \(\rm HCl\) 蒸发结晶 \(\xcancel{\rm CaCl_2}\) \(\xcancel{\rm CaCO_3 \darr}\) \(\xcancel{\rm MgCl_2}\) \(\xcancel{\rm Mg(OH)_2 \darr}\) \(\xcancel{\rm Na_2SO_4}\) \(\xcancel{\rm BaSO_4 \darr}\) \(\xcancel{\rm BaCl_2}\) \(\xcancel{\rm BaCO_3 \darr}\) \(\xcancel{\rm Na_2CO_3}\) \(\xcancel{\rm H_2O+ CO_2 \uarr}\) \(\xcancel{\rm NaOH}\) \(\xcancel{\rm H_2O}\) \(\xcancel{\rm HCl}\) -
过量 \(\rm BaCl_2\) \(\rarr\) 过量 \(\rm NaOH\) \(\rarr\) 过量 \(\rm Na_2CO_3\) \(\rarr\) 过滤 \(\rarr\) 过量稀盐酸 \(\rarr\) 蒸发结晶
-
过量 \(\rm NaOH\) \(\rarr\) 过量 \(\rm BaCl_2\) \(\rarr\) 过量 \(\rm Na_2CO_3\) \(\rarr\) 过滤 \(\rarr\) 过量稀盐酸 \(\rarr\) 蒸发结晶
注意:过量的 \(\rm BaCl_2\) 需要 \(\rm Na_2CO_3\) 除去,所以先加 \(\rm BaCl_2\) 再加 \(\rm Na_2CO_3\)
\(\boxed{碳酸在钡后,盐酸在最后}\)
滤渣中有 \(4\) 中沉淀:\(\rm CaCO_3, BaSO_4, Mg(OH)_2, BaCO_3\)
试剂的作用:① \(\rm Na_2CO_3\) 溶液:除去杂质中的 \(\rm CaCl_2\) 和 过量的 \(\rm BaCl_2\) ② 稀盐酸:去除过量的 \(\rm NaOH\) 和 \(\rm Na_2CO_3\)
物质除杂
物理方法
过滤、结晶(蒸发结晶、降温结晶)
化学方法
- 沉淀法:\(\rm KCl(K_2SO_4)\) 加入适量 \(\rm BaCl_2\) 溶液,过滤
- 气化法:\(\rm KCl(K_2CO_3)\) 加入适量稀盐酸
- 加热法:\(\rm CaO(CaCO_3)\) 高温煅烧至固体质量不再改变
- 置换法:\(\rm FeSO_4(CuSO_4)\) 加入过量铁粉,过滤
- 溶解法:\(\rm Cu(Fe)\) 加入适量稀硫酸,过滤
例:\(\rm NaOH溶液(Ba(OH)_2)\)
解:① 确定杂质离子 \(\rm Ba^{2+}\) ②确定除杂所需离子 \(\rm SO_4^{2-}\) ③ 确定除杂所需试剂 \(\rm Na_2SO_4\)
④ \(\rm Ba(OH)_2 + Na_2SO_4 \xlongequal{\ \ \ \ } 2NaOH + BaSO_4 \darr\)
除杂原则(不增、不减、易分解)
-
不能引入新的杂质
-
所选用的物质能够除去杂质且不能与原物质反应
例:\(\rm NaOH(Na_2CO_3)\) 用 \(\rm HCl\) 不能除杂
-
反应后杂质易与原物质分离
-
保持原物质的状态
例:\(\rm NaCl固体(CaCO_3)\) 加水过滤后应将 \(\rm NaCl\) 溶液蒸发为固体



 浙公网安备 33010602011771号
浙公网安备 33010602011771号