EULAR25_OP0327_eRA的GC桥接后减停
早期RA中糖皮质激素的减量和停用:复发的风险[北欧五国]
关键词:减量、疾病修饰药物(DMARDs)、结局评估、随机对照试验、糖皮质激素
小结: 利用北欧五国NORD-STAR数据, 分析发现早期RA采用口服GC作为桥接治疗并逐步减停GC后的总第40周病情复发风险显著高于生物制剂或经关节腔注射GC组.

背景:
RA患者常出现病情复发,有时与治疗方案的改变有关。国际建议主张将糖皮质激素(GC)主要用于传统合成DMARDs(csDMARDs)起效之前的桥接治疗,以尽量减少长期使用GC的不良影响[1]。然而,尚未有研究探讨GC桥接治疗是否会增加后续复发的风险,即通过临床疾病活动指数(CDAI)评分的绝对变化来定义。
目的:
研究在早期RA中,初始口服GC治疗的减量和停用,以及与bDMARDs治疗相比,初始GC注射治疗后的复发风险。
方法:
本研究使用了在瑞典、丹麦、挪威、芬兰、荷兰和冰岛开展的NORD-STAR试验的数据(NCT01491815)[2]。CDAI复发被定义为自上次访视以来增加至少4.5分[3]。NORD-STAR试验的活性传统治疗组1A(“口服组”)接受甲氨蝶呤联合口服GC(起始剂量为每天20mg,第9周减量至5mg,并按照方案在第36周停用);活性传统治疗组1B(“注射组”)接受三联疗法(甲氨蝶呤、柳氮磺胺吡啶、羟氯喹)以及对肿胀关节进行强制性关节内GC注射(每次最多4个关节或每次最多4mL)。生物制剂组接受甲氨蝶呤联合一种生物制剂(培塞利珠单抗、阿巴西普或托珠单抗)。在所有治疗组中,当临床需要时允许进行关节腔内GC注射(但第20-24周和第44-48周期间除外)。生物制剂组作为口服组(GC有减量和停用)和注射组(无方案变更)的对照组。首先使用逻辑广义估计方程(GEE)对复发率进行纵向分析。此外,对于在48周前停用GC的口服亚组患者,使用逻辑回归分析评估停用GC后下次随访时的复发风险,并与生物制剂组中年龄、性别和周次匹配的对照组以及注射组中性别和周次匹配的患者进行比较。分析校正了性别、抗环瓜氨酸肽抗体(ACPA)状态、国家、年龄、体重指数(BMI)、基线时的DAS28-CRP和吸烟状态。
结果:
本亚研究共纳入810例随机患者:口服组135例,注射组80例,生物制剂组595例。在48周或提前终止期间,口服组130例患者中有56例(43%)、注射组75例患者中有18例(24%)、生物制剂组565例患者中有160例(28%)至少出现一次复发。在纵向GEE分析中,口服组随时间(12、24、32、40和48周)出现CDAI增加定义的复发风险高于生物制剂组(比值比:1.62[95%置信区间:1.18-2.22])。在各个时间点上,口服组的风险在所有访视中均数值更高,且在第40周(比值比:2.58[95%置信区间:1.45-4.61])显著更高,这是方案规定的停用GC后的访视,与生物制剂组相比。相比之下,接受GC注射治疗的患者随时间的复发率与生物制剂组相似(比值比:0.92[95%置信区间:0.52-1.63],图1A),尽管大多数关节内注射是在研究早期进行的(表1)。我们观察到,在48周时,口服组135例患者中有71例(53%)按计划停用了GC并继续留在试验中。在这些患者中,停用GC后的下次随访时复发风险更高(比值比:2.47[95%置信区间:1.10-5.54]),与匹配的生物制剂对照组相比(图1B)。
结论:
对于在48周时停用了口服GC并继续留在试验中的患者,与生物制剂治疗相比,停用长期口服GC桥接策略后,CDAI定义的复发风险显著更高。初始关节内注射可能具有长期效应,因为注射组的复发率与生物制剂治疗相似。在为RA选择长期、低剂量GC桥接策略时,必须考虑停用后复发风险增加的问题。
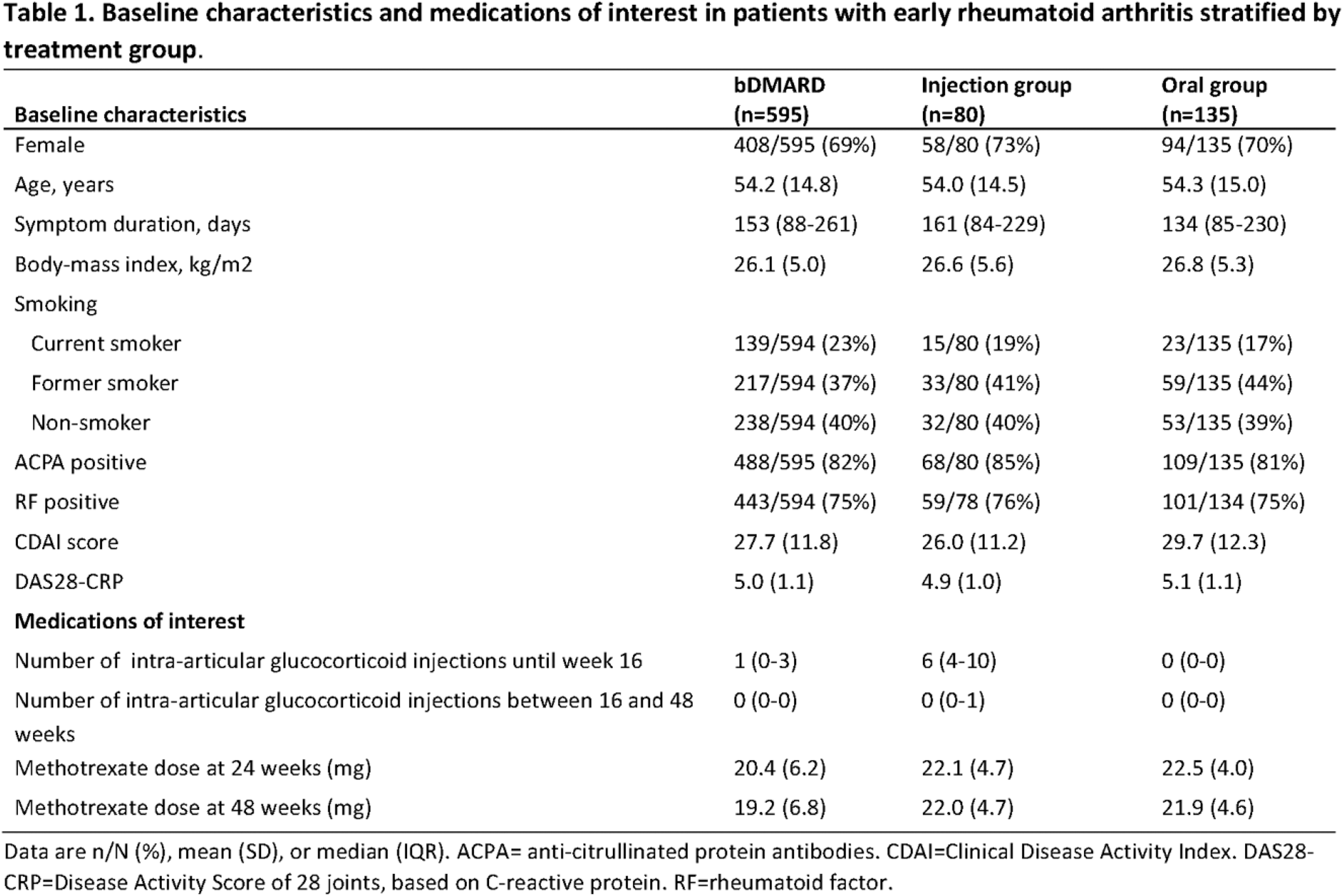
表1. 按治疗组分层的早期RA患者的基线特征和相关用药情况
参考文献
[1] Smolen, J.S., et al., EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Ann Rheum Dis, 2023. 82 (1): p. 3-18.
[2] Østergaard, M., et al., Certolizumab pegol, abatacept, tocilizumab or active conventional treatment in early rheumatoid arthritis: 48-week clinical and radiographic results of the investigator-initiated randomised controlled NORD-STAR trial. Ann Rheum Dis, 2023. 82 (10): p. 1286-1295.
[3] Konzett, V., et al., Definition of rheumatoid arthritis flare based on SDAI and CDAI. Ann Rheum Dis, 2024. 83 (2): p. 169-176.
致谢:我们对参与NORD-STAR试验的患者、研究护士、研究人员、关节评估员、数据管理人员和研究团队表示衷心的感谢。
利益冲突声明:Kristina Lend、Jos W.R.Twisk、Frieda Koopman、Anna Rudin:无利益冲突声明。Merete Lund Hetland:从AbbVie、Bristol Myers Squibb、Eli Lilly、MSD、Pfizer、Sandoz、Novartis、Nordforsk和UCB获得机构资助;从Medac、Novartis、Pfizer、Sandoz和UCB获得演讲费;从AbbVie获得机构数据安全监测委员会或顾问委员会费用。MLH主持了丹麦风湿病质量登记处(DANBIO,DRQ)的指导委员会,该登记处从医院所有者获得公共资金和制药公司的资助。MLH共同主持EuroSpA,该组织基于二次数据生成治疗银屑病关节炎和轴性脊柱关节炎的真实世界证据,部分由Novartis和UCB资助。Till Uhlig:从Lilly、Pfizer、UCB和Galapagos获得演讲费。Dan Nordström:从Bristol Myers Squibb、Lilly、Novartis、Pfizer和UCB获得研究资助;从Pfizer和UCB获得演讲费;从UCB获得数据安全监测委员会或顾问委员会费用。Michael Nurmohamed、Bjorn Gudbjornsson、Kim Hørslev-Petersen、Marte S Heiberg、Tuulikki Sokka-Isler、Gerdur Grondal:无利益冲突声明。Espen A Haavardsholm:从Pfizer、UCB和Novartis获得个人演讲费;从AbbVie、Pfizer和Eli Lilly获得数据安全监测委员会或顾问委员会费用。Mikkel Østergaard:从AbbVie、BMS、Boehringer-Ingelheim、Celgene、Eli-Lilly、Galapagos、Gilead、Hospira、Janssen、Merck、Novartis、Pfizer、Sandoz和UCB获得研究资助;从AbbVie、Amgen、BMS、Merck、Celgene、Eli Lilly、Novartis和UCB获得演讲费。Jon Lampa:无利益冲突声明。Ronald F.van Vollenhoven:从AbbVie、AstraZeneca、Biogen、Bristol Myers Squibb、Galapagos、GSK、Janssen、Pfizer、RemeGen和UCB获得研究或教育的机构资助。



 浙公网安备 33010602011771号
浙公网安备 33010602011771号