易基因:Adv Sci/IF14.1:中科院动物所郭帆团队等表观多组学揭示克隆胚胎DNA羟甲基化动态及功能 解析体细胞重编程障碍机制
大家好,这里是专注表观组学十余年,领跑多组学科研服务的易基因。
2025年11月18日,安徽医科大学第一附属医院梁丹教授团队和中国科学院动物研究所郭帆研究员团队合作,首次系统绘制了小鼠体细胞核移植(SCNT)克隆胚胎植入前发育完整阶段的全基因组5-羟甲基胞嘧啶(5hmC)动态图谱,并通过联合全基因组重亚硫酸盐测序(WGBS)、APOBEC偶联表观遗传测序(ACE-seq)及RNA测序(Smart-seq2)等多组学技术,共同揭示了5hmC异常修饰模式在克隆胚胎发育障碍中的关键作用。本研究发现,SCNT胚胎在2细胞期呈现出一种独特的"类精子但减弱"的亲本等位基因对称性5hmC分布模式,这一特征显著区别于自然受精胚胎的亲本不对称模式;雌性克隆胚胎X染色体5hmC沉积显著不足,而生殖印记控制区(gICRs)则表现出去甲基化(5hmC相关)抵抗。此外,进一步的TET3过表达实验表明,TET3过表达介导5hmC水平异常升高,从而导致发育相关基因过早激活并严重阻碍克隆胚胎发育。该研究不仅阐明了5hmC在体细胞重编程中的精确调控机制,也为提升哺乳动物克隆效率提供了新的理论靶点。相关研究成果以“5-Hydroxymethylcytosine Dynamics Reveals Coordinated Reprogramming of Parental Genomes and X Chromosome Dosage Balance in Mouse SCNT Embryos“为题发表于《Advanced Science》期刊。

标题:5-Hydroxymethylcytosine Dynamics Reveals Coordinated Reprogramming of Parental Genomes and X Chromosome Dosage Balance in Mouse SCNT Embryos(5-羟甲基胞嘧啶动态揭示小鼠SCNT胚胎亲本基因组的协同重编程与X染色体剂量平衡)
发表时间:2025年11月18日
发表期刊:Advanced Science
影响因子:IF14.1/Q1
技术平台:WGBS、ACE-seq、Smart-seq2(易基因金牌技术)
作者单位:安徽医科大学第一附属医院、中国科学院动物研究所
DOI:10.1002/ADVS.202509682
这一研究以体细胞核移植(Somatic Cell Nuclear Transfer,SCNT)胚胎表现出以DNA甲基化异常为主要表征的广泛表观遗传突变为方向,发现DNA 5-羟甲基胞嘧啶(5hmC)参与早期胚胎发育过程中的甲基化重编程。研究团队通过系统性地绘制了小鼠SCNT胚胎亲本等位基因的特异性全基因组5hmC图谱发现2细胞期供体体细胞的双亲本基因组短暂性获得类似正常受精胚胎中父本基因组的对称性羟甲基化模式,但整体信号明显较弱且快速消退;尤其是在母本基因组克隆胚胎中,X染色体羟甲基化严重不足,而多个关键生殖印记控制区(germline imprinting control regions,gICRs)表现出较强去甲基化抵抗的模式。尽管新生5hmC生成与体细胞-受精卵转换过程中的初始DNA去甲基化密切相关,但其与持续的甲基化变化随后发生解耦。有趣的是,通过Tet3过表达提升全局5hmC水平会导致发育有关基因在2细胞期过早激活,从而导致SCNT胚胎发育失败不良结局。这些发现通过揭示SCNT胚胎中异常5hmC重编程的独特动态及其功能结局,完善哺乳动物克隆胚胎发育过程精准的DNA羟甲基化调控的相关机制。
易基因相关拓展性产品案例
- 项目文章|微量WGBS+ACE-seq揭示卵巢早衰的人卵丘细胞DNA甲基化与羟甲基化表观基因组图谱
- 项目文章|Nature子刊:RRBS等揭示IDH1-R132H突变通过DNA甲基化加剧顺铂诱导肾毒性
- 项目文章|DNA(羟)甲基化研究揭示铁离子依赖表观调控促进狼疮致病性T细胞分化
- 项目文章|Sci Adv:WGBS+ChIP-seq揭示DNA甲基化在异基因造血干细胞移植后延迟血小板恢复中的关键作用
- 项目文章|JAR (IF13):西农陈玉林团队多组学分析揭示绵羊早期胚胎发育的分子与表观遗传调控机制
研究方法
胚胎模型构建:以杂交小鼠(C57BL/6J × PWK/PhJ)的E13.5胎鼠成纤维细胞(MEFs)为核供体,构建SCNT胚胎,并分阶段(2细胞期、4-8细胞期、囊胚期)收集样本。
多组学测序技术:
- ACE-seq:通过ACE-seq测序,单碱基分辨率检测5hmC全基因组分布。
- WGBS:全基因组甲基化测序,与ACE-seq数据联合分析5mC/5hmC动态关联。
- RNA-seq:Smart-seq2技术分析基因表达,关联5hmC修饰与转录调控。
等位基因特异性分析:利用杂交小鼠SNP区分亲本基因组,解析亲本特异性表观遗传模式。
功能验证:通过TET3过表达(mTet3-plus mRNA注射)提升5hmC水平,观察其对发育的影响。
数据整合:整合WGBS和ACE-seq数据,精准量化5mC/5hmC/未修饰胞嘧啶比例。
结果图形
(1)SCNT胚胎发育过程中的5hmC全基因组图谱
本研究首先构建了SCNT胚胎从供体MEF至囊胚期发育过程中的完整5hmC动态图谱(图1A)。通过整合WGBS与ACE-seq数据,研究者发现整体5hmC水平在2细胞期出现显著峰值,随后在4-8细胞期逐渐下降,至囊胚期达最低点,呈现"先升后降"的独特动态模式(图1B-C)。具体而言,在体细胞-受精卵转换(SZT)期间,高5hmC CpG位点比例及基因本体(gene body)区域的5hmC信号均显著增强。值得注意的是,SCNT胚胎的DNA甲基化动态表现为"去甲基化-de novo甲基化-二次去甲基化"的双波模式,与5hmC的"单峰"模式形成鲜明对比(图1C)。研究进一步将78,732个差异羟甲基化区域(DhMR)分为四类:25,516个新生成5hmC位点、2,820个丢失5hmC位点、15,737个持续高5hmC位点及34,659个持续低5hmC位点(图1D)。基因组特征分析显示,新生成及稳定高5hmC区域显著富集于增强子、基因本体及H3K36me3/H3K27ac/H3K4me3修饰区域(图1E-F),这表明5hmC沉积偏好转录活跃的调控元件。
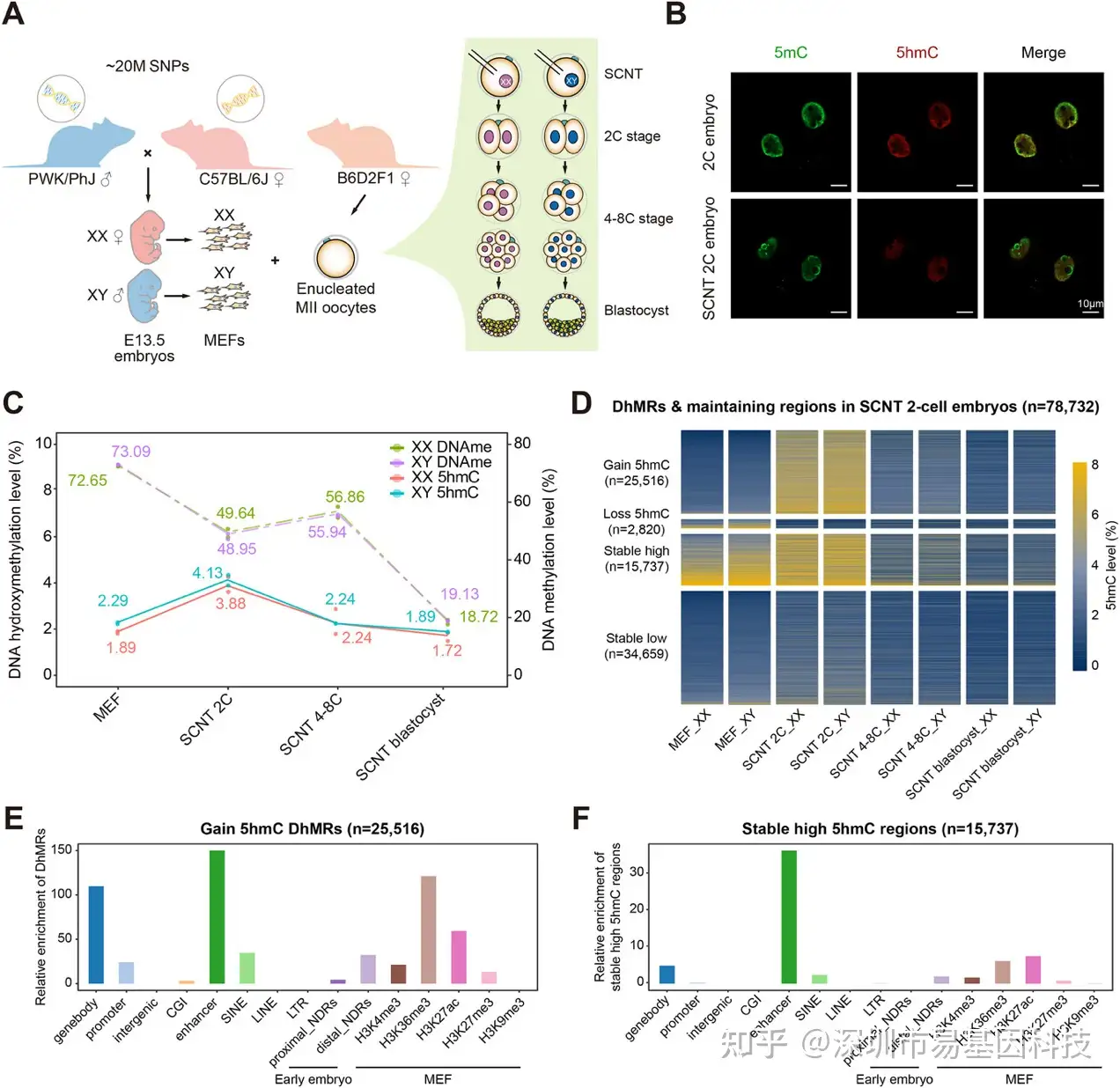
图1:SCNT胚胎发育过程中细胞核5hmC的全基因组动态图谱
(2)5hmC参与SCNT胚胎第一次DNA去甲基化
研究深入探究了5hmC与5mC动态的相关性,发现5hmC与5mC在SZT转换阶段(MEF至2细胞期)存在特异性负相关(图2D-E)。在2细胞期,发生去甲基化的DMRs伴随显著的5hmC生成,而维持高甲基化的区域则未见5hmC积累(图2B-C)。值得注意的是,这种耦联关系在后续发育阶段(2细胞至4-8细胞期、4-8细胞至囊胚期)完全消失,5hmC水平在不同甲基化动态区域间无差异。ACE-seq研究证实第一次去甲基化与5hmC生成紧密相关,而第二次去甲基化及de novo甲基化则不依赖于5hmC调控。
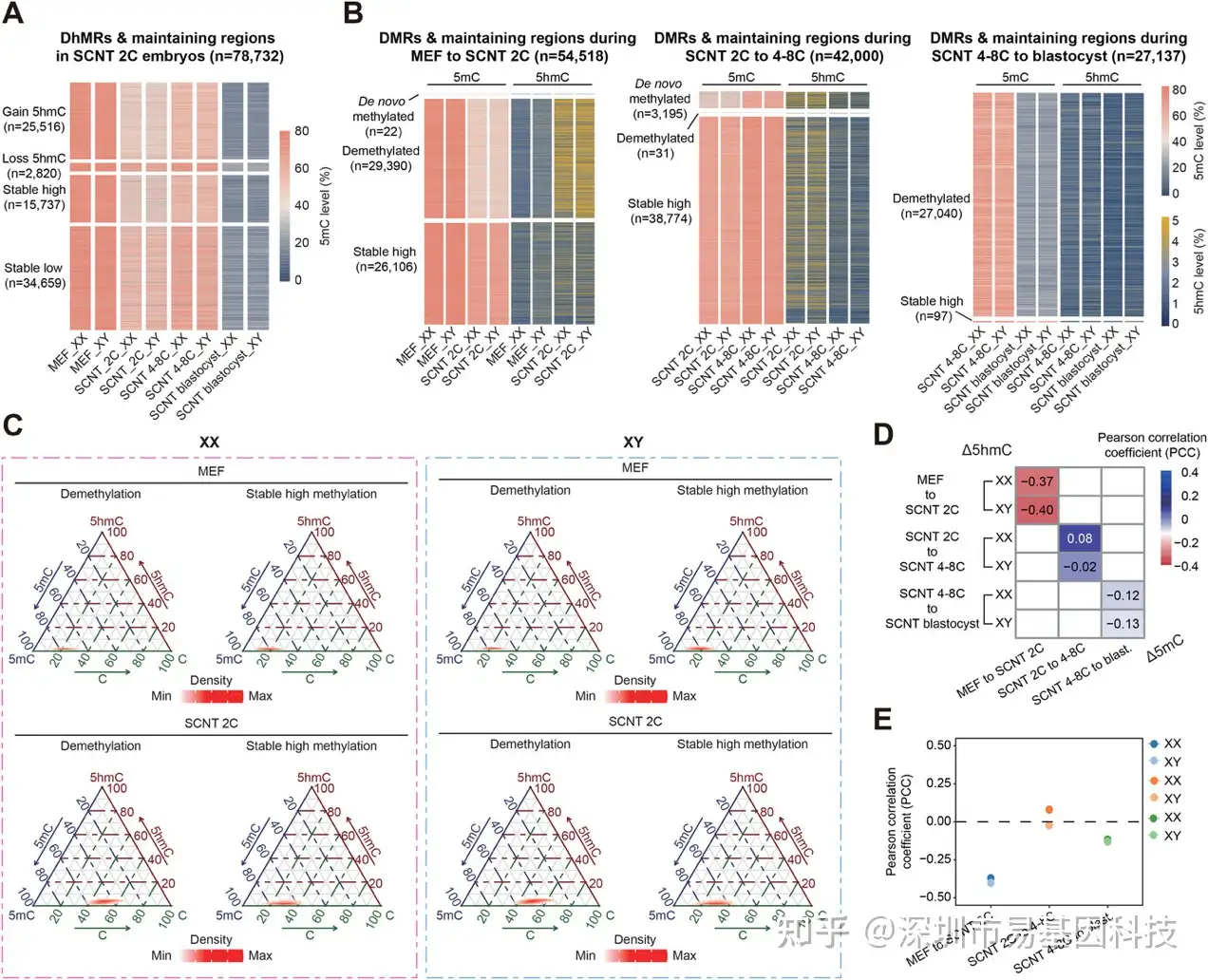
图2:SCNT囊胚前DNA羟甲基化与DNA甲基化动态的相关性
(3)SCNT胚胎生殖印记控制区的5hmC动态
17个母本gICRs分析显示,SCNT胚胎在2细胞至4-8细胞期维持高甲基化状态,但在囊胚期第二次去甲基化中出现显著5hmC非依赖性印记丢失(图3A-B)。相关性分析验证结果揭示gICRs甲基化与5hmC水平在母本等位基因上无显著关联(图3C-D),表明印记区域存在特殊的保护机制抵抗TET3介导的氧化。上述研究结果表明gICRs去甲基化机制不依赖于羟甲基化动态变化。
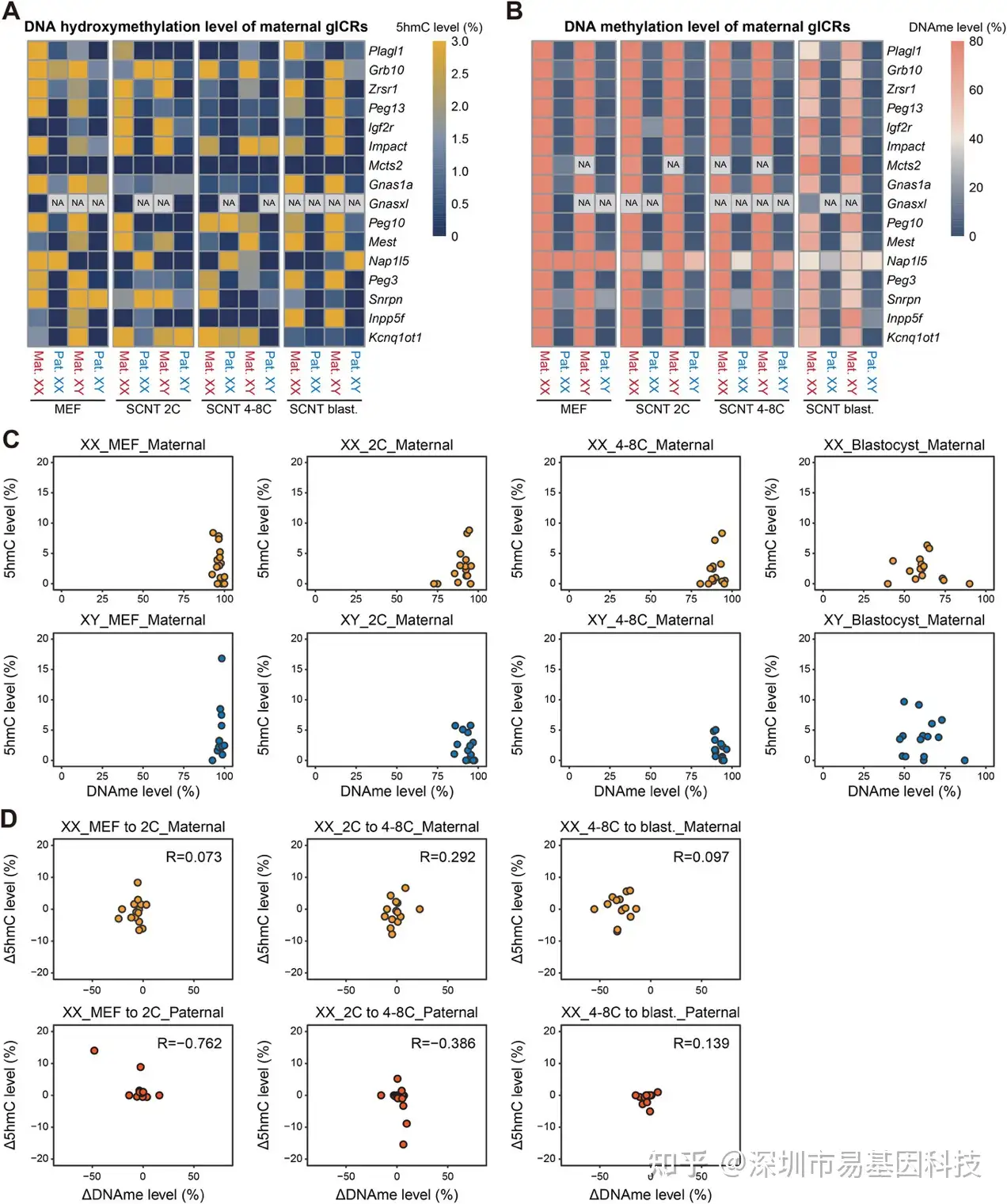
图3:母本gICR在SCNT发育过程中的5hmC水平变化。
(4)SCNT胚胎亲本基因组X染色体的5hmC积累
X染色体剂量补偿分析揭示了SCNT胚胎最显著的性别特异性缺陷(图4A)。在2细胞期,雌雄胚胎的常染色体5hmC水平在亲本等位基因间对称分布,但X染色体5hmC显著低于常染色体;雌性胚胎的亲本X染色体5hmC显著低于常染色体和雄性胚胎的单一母本X染色体(图4B)。该现象排除了MEF供体细胞的遗传继承(图4E),证实是SZT重编程过程中5hmC生成不足所致。值得注意的是,SCNT胚胎Xist基因在雌性中显著异常高表达(图4C),但X染色体/常染色体转录比例在雌雄间无差异(图4D),提示不足的5hmC可能通过维持高甲基化(图4G)来促进Xist异常激活,这可能破坏X染色体剂量补偿机制。与野生型(WT)2细胞期胚胎相比,WT中X染色体5hmC水平与常染色体相当(图4F),揭示SCNT胚胎X染色体的"羟甲基化缺陷"具有克隆特异性。
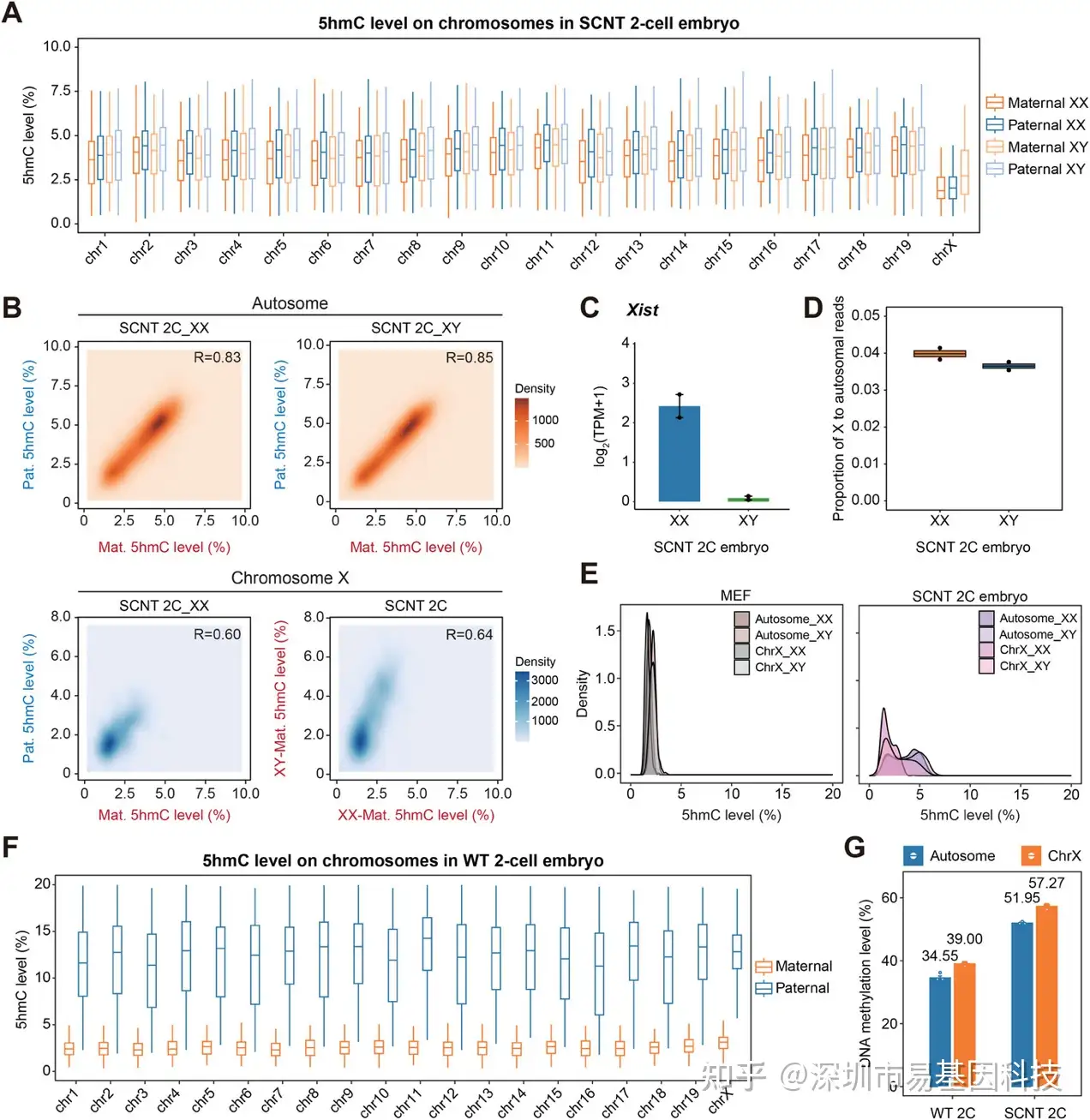
图4:雄雌胚胎及X染色体与常染色体之间的5hmC分布差异
(5)异常5hmC分布与SCNT发育障碍的相关性
比较SCNT与WT胚胎发现,尽管受精卵5hmC起始水平低于体细胞,WT在2细胞期胚胎5hmC总量仍显著高于SCNT(图5A),表明重编程效率不足。SCNT特异性高甲基化在4-8细胞期尤为突出(图5A)。通过整合已发表WT胚胎数据,研究鉴定出四类DhMRs:SCNT特异区、WT特异区、共有高5hmC区和共有低5hmC区(图5B)。其中,SCNT特异5hmC区域羟甲基化升高,且伴随比WT更高的甲基化水平,提示"不完全重编程"状态。基因组特征分析显示,两类细胞特异性DhMRs均富集于增强子(图5C),且SCNT特异增强子关联基因显著下调,而WT特异增强子关联基因富集于细胞命运决定、模式形成等早期发育通路(图5D-E)。
通过RNA测序Smart-seq2提供的高灵敏度转录组数据与ACE-seq测序绘制的增强子5hmC信号图谱进行邻近关联分析,共鉴定出779个SCNT特异基因和1,047个WT特异基因。这种多组学联用策略揭示,SCNT胚胎并非整体5hmC缺失,而是在关键发育增强子上"异位不足",导致ZGA(合子基因组激活)相关发育程序未能正常启动,从而导致发育失败。
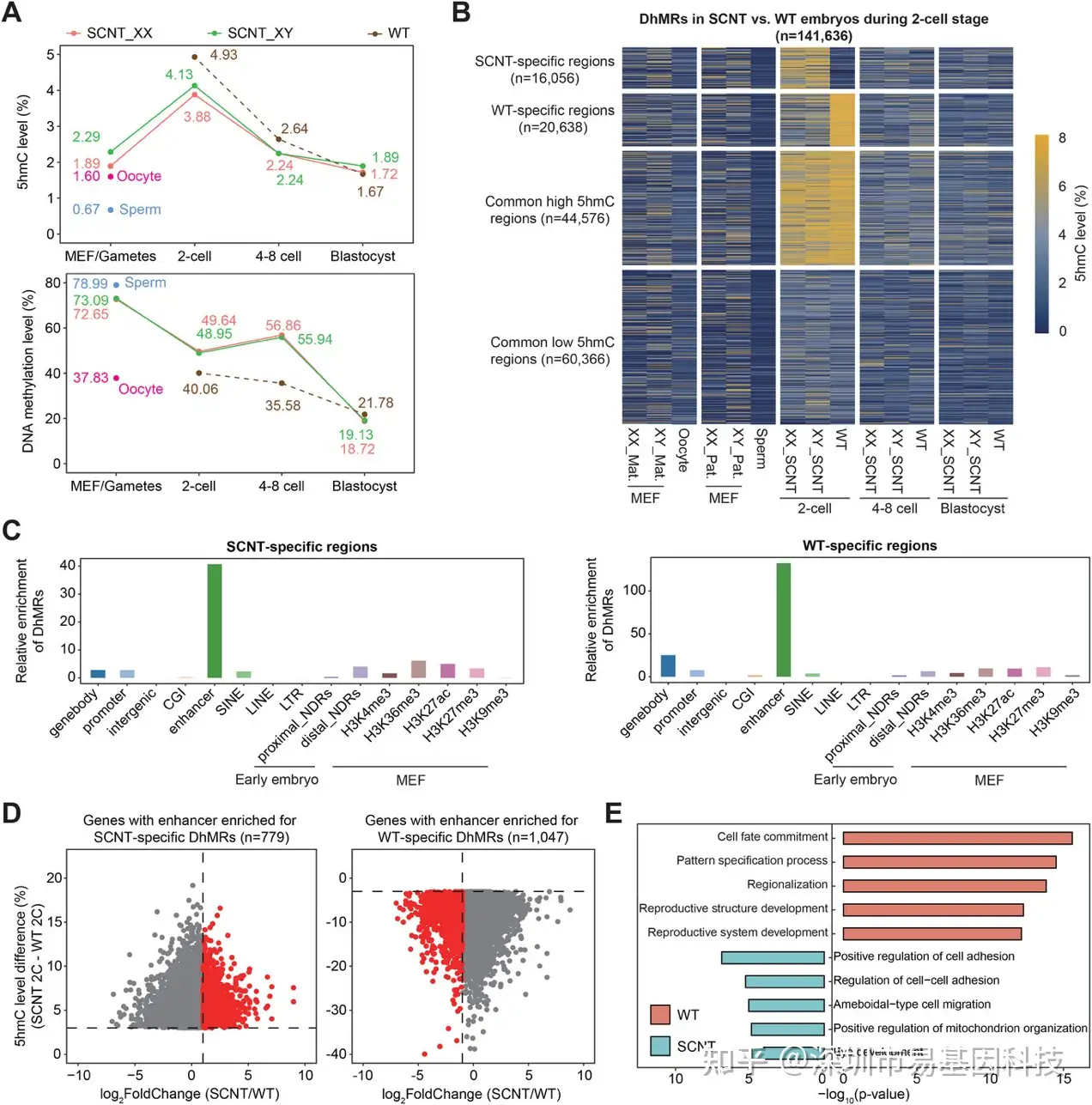
图5:2细胞期WT胚胎与SCNT胚胎5hmC分布比较
(6)SCNT胚胎亲本等位基因特异性5hmC动态
等位基因分辨率分析揭示了SCNT胚胎发育失败的特异性模式(图6A-B)。WT在2细胞期胚胎父本基因组5hmC达13.3%,母本仅2.69%,呈现典型不对称分布;而SCNT的雌雄胚胎均表现为亲本等位基因对称(约4-5%)(图6A)。在100 kb基因组范围内上,SCNT双亲本基因组的5hmC水平与彼此高度线性相关,且整体分布模式类似WT父本基因组但强度减弱(图6C-D)。t-SNE降维分析显示,SCNT 2细胞亲本基因组聚类于WT父本基因组附近,而远离WT母本基因组(图6E),表明无论DNA来源,卵胞质促进了"类精子"重编程。DNA甲基化分析显示类似对称性,且SCNT基因组从MEF到2细胞的甲基化水平和分布与WT精子到2细胞的父本基因组变化呈强线性相关,但去甲基化程度普遍更低。
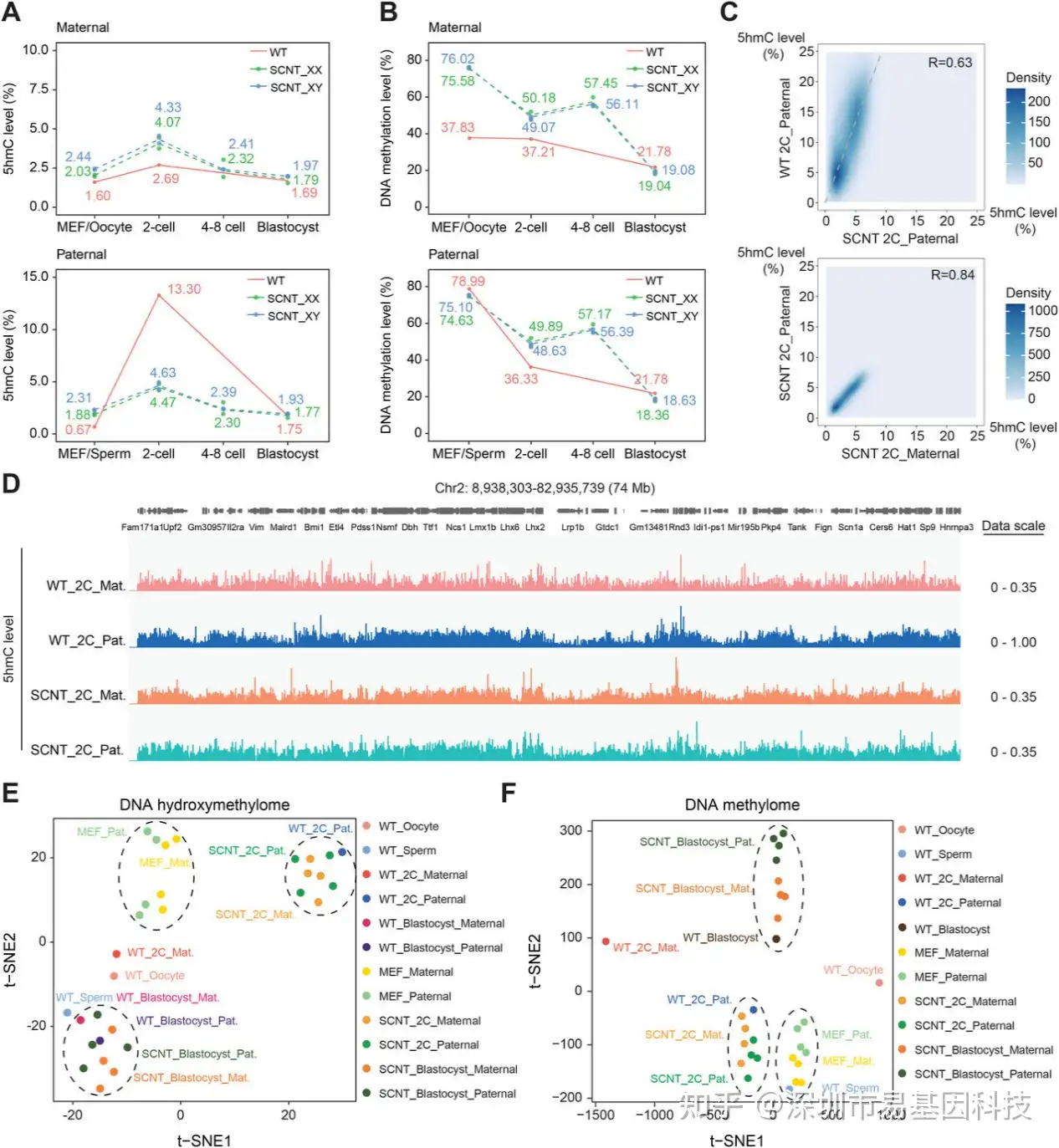
图6:SCNT胚胎与受精胚胎父本和母本基因组5hmC分布比较
(7)高5hmC破坏SCNT胚胎表观遗传谱
为验证5hmC功能,研究在SCNT胚胎中过表达mTet3-plus突变体(图7A)。免疫荧光证实HA标签蛋白表达(图7B),整体5hmC水平在2细胞期升至11.49%,远高于对照的4.13%(图7C),且高5hmC CpG比例及亲本等位基因信号均显著增加。分析发现43,736个位点发生5hmC新生成,其中33,380个为"异位生成"(即在正常SCNT中不羟甲基化)(图7D)。这些新生成位点强烈富集于增强子、H3K27me3/H3K36me3修饰区(图7E)。去甲基化DMRs在过表达组中5hmC显著升高(图7F),验证了高5hmC与去甲基化正相关。然而,即使整体5hmC提升,亲本基因组仍保持对称性(图7G),且雌性X染色体5hmC仍显著低于常染色体(图7H),说明X染色体抵抗不可单纯通过TET3活性增强而克服。值得注意的是,过高5hmC并未改善SCNT胚胎发育,反而加剧阻滞,提示5hmC并非"越多越好",其时空分布精确性至关重要。
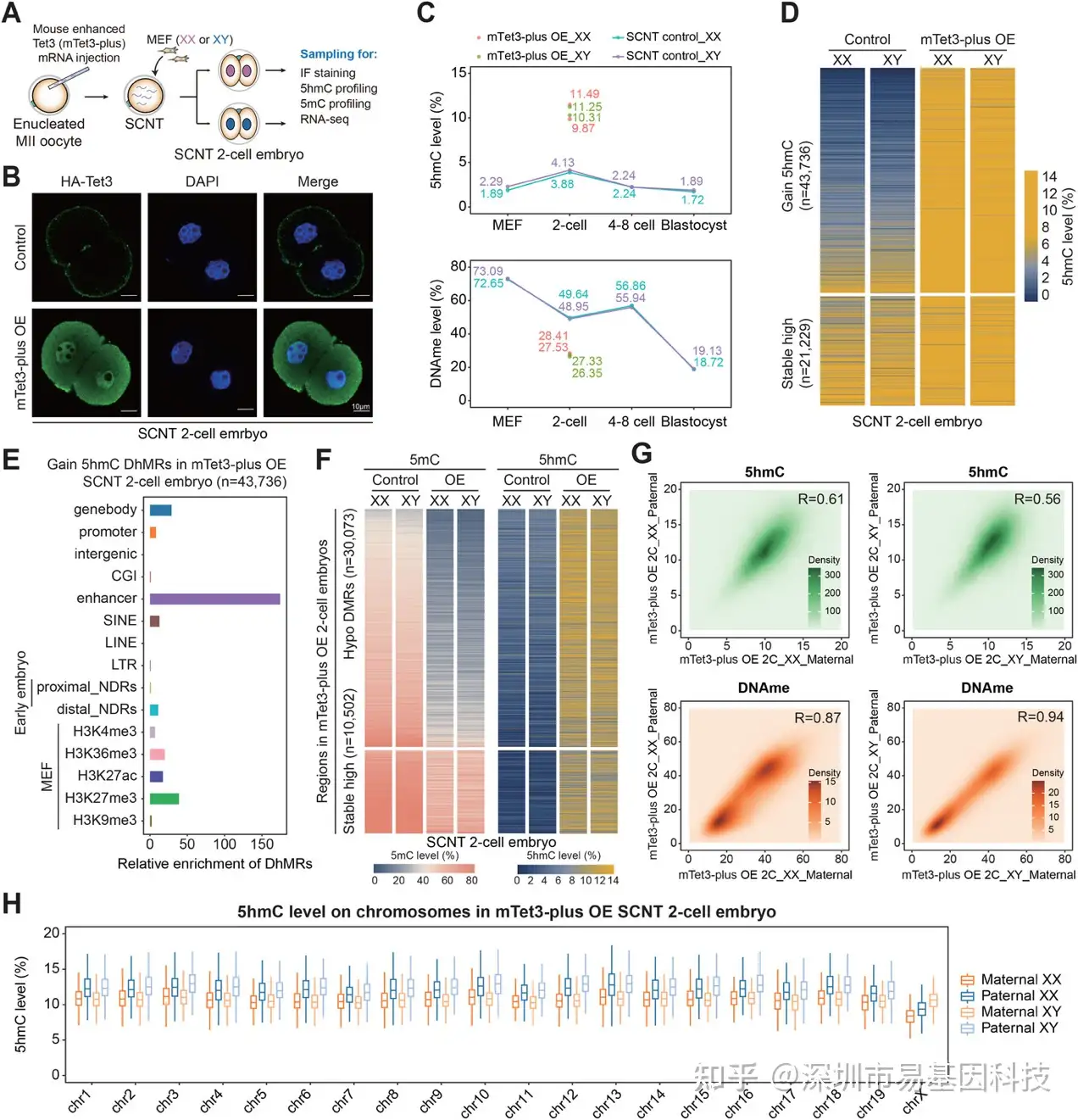
图7:Tet3过表达SCNT胚胎中5hmC的水平与分布
(8)异位5hmC生成导致基因过早激活并阻碍SCNT胚胎发育潜能
mTet3-plus过表达胚胎中,母本gICRs在2细胞期出现印记丢失(图8A),而正常SCNT中此过程延迟至囊胚期,说明异位5hmC可突破印记保护。在SCNT中沉默/低表达且在过表达基因组中激活,且启动子区5hmC异位生成伴去甲基化的胚胎中鉴定出雌性597个、雄性753个异常再激活基因(图8D)。GO分析显示这些基因富集于"模式特化"、"区域化"、"成骨化"等原肠运动后事件(图8E-F),表明2细胞期不应表达的晚期发育基因被过早激活。发育追踪显示,无论100、200或500 ng/μL剂量,mTet3-plus过表达均显著降低2细胞分裂率及囊胚形成率(图8G)。研究最终证明,5hmC的"精准调控"而非"整体提升"是SCNT成功的关键,异位羟甲基化会时序错乱地激活发育程序,导致胚胎在合子基因组激活(ZGA)阶段即失去发育协调性。
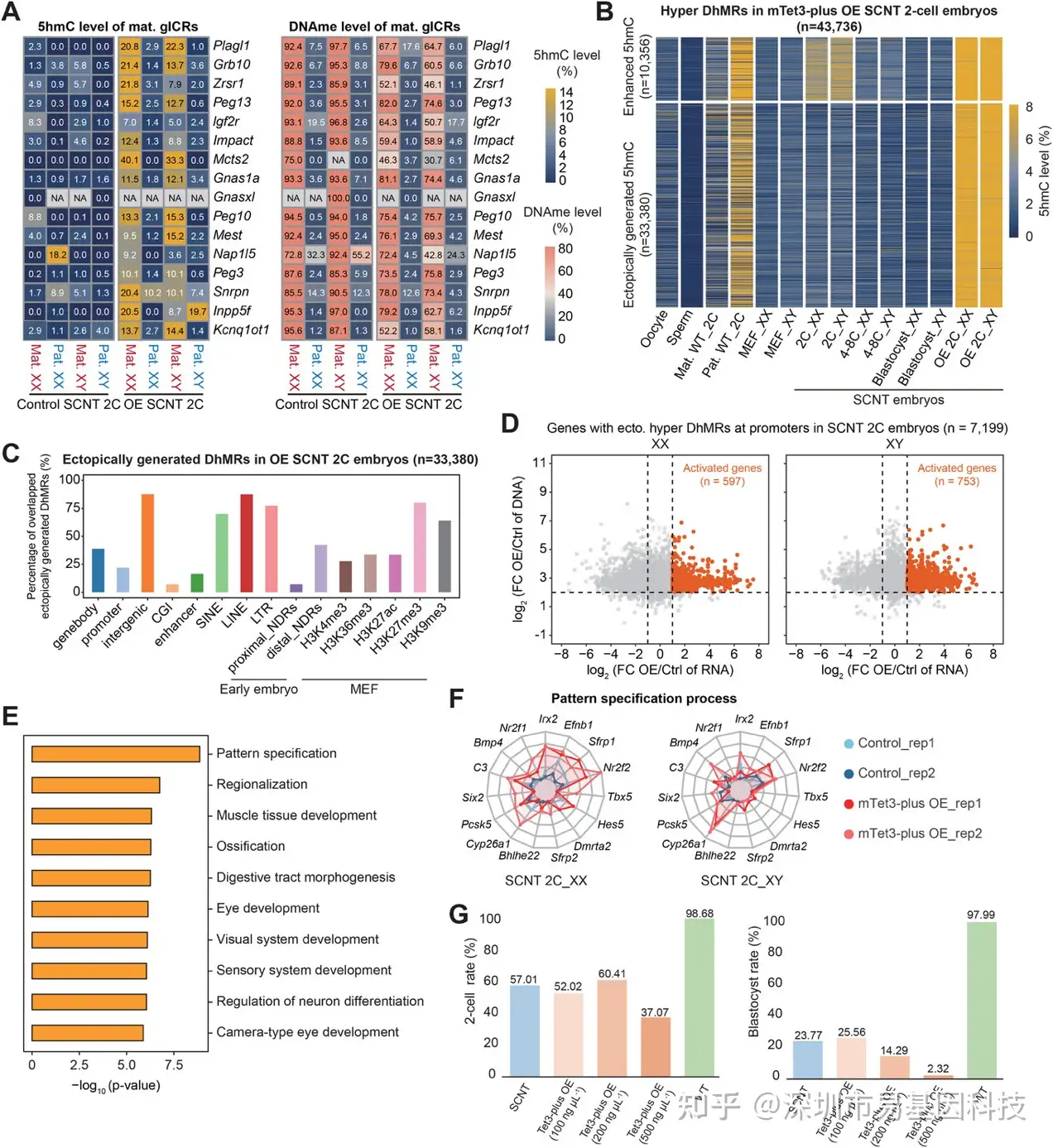
图8:SCNT胚胎中5hmC动态与分布特征的示意图
结论和启示
本研究通过创新的多组学技术整合,系统阐明了5hmC是小鼠SCNT胚胎重编程的关键表观障碍,其异常表现为"时间错位、空间错误、剂量失准"。主要结论包括:
(1)SCNT胚胎在2细胞期建立了一种非生理的亲本等位基因对称5hmC分布,丧失自然受精中父本特异性高羟甲基化模式;
(2)雌性X染色体5hmC严重不足是导致剂量补偿失败的重要原因;
(3)印记区对5hmC介导的去甲基化具有抵抗性,但在囊胚期发生延迟性印记丢失;
(4)5hmC生成与第一次DNA去甲基化耦联,但后续解耦,提示重编程存在一个关键时间窗口;
(5)全局提升5hmC水平反而导致发育基因过早激活和胚胎致死,证实精准调控的必要性。
本研究在多组学方案(WGBS+ACE-seq+RNA-seq)上的成功应用,为解析表观遗传障碍提供了全新视角,可广泛应用于早期胚胎、疾病模型等表观遗传研究,尤其适用于微量样本的高分辨率分析。
易基因DNA甲基化整体研究方案
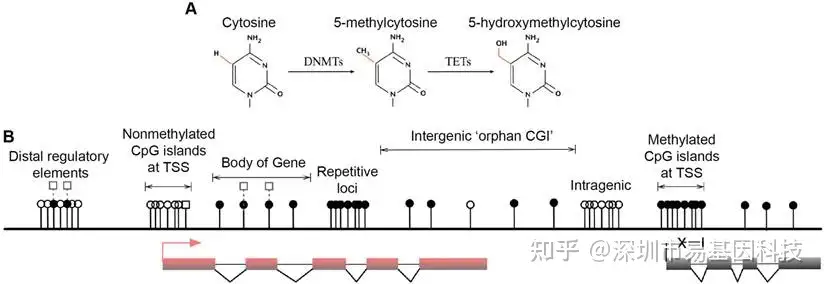
DNA甲基化是一种表观遗传修饰,指DNA分子在DNA甲基转移酶的作用下将甲基选择性地添加到特定碱基上的过程。主要发生在胞嘧啶的CpG位点,也可以在非CpG位点和CpG岛中发生。DNA甲基化参与调控基因表达、X染色体失活、基因印记、胚胎发育、细胞分化、肿瘤发生以及维持基因组稳定性。
参考文献:
Xiang Z, Yan R, Guo J, Wang M, Cheng X, Zhang F, Guo T, Long X, Guo F, Liang D. 5-Hydroxymethylcytosine Dynamics Reveals Coordinated Reprogramming of Parental Genomes and X Chromosome Dosage Balance in Mouse SCNT Embryos. Adv Sci (Weinh). 2025 Nov 18:e09682. doi: 10.1002/advs.202509682.
相关阅读:
1.项目文章|JAR (IF13):西农陈玉林团队多组学分析揭示绵羊早期胚胎发育的分子与表观遗传调控机制
2.项目文章|多组学分析揭示坏死性小肠结肠炎(NEC)的新型DNA甲基化调控生物标志物及发病机制
3.项目文章|中山大学凌文华团队DNA甲基化研究揭示血管衰老与动脉粥样硬化的表观调控机制
4.项目文章|Sci Adv:WGBS+ChIP-seq揭示DNA甲基化在异基因造血干细胞移植后延迟血小板恢复中的关键作用
5.项目文章|WGBS揭示Vpr蛋白在HIV-1感染中对CD4+ T细胞DNA甲基化变化的作用
6.项目文章|微量WGBS+ACE-seq揭示卵巢早衰的人卵丘细胞DNA甲基化与羟甲基化表观基因组图谱
8.技术推介|DNA羟甲基化研究:APOBEC-coupled epigenetic sequencing(ACE-Seq)


 浙公网安备 33010602011771号
浙公网安备 33010602011771号