易基因:Blood/IF23.1:徐州医科大学牛铭山团队揭示多发性骨髓瘤免疫逃逸介导CAR-T耐药的遗传与表观遗传调控双重机制|项目文章
大家好,这里是专注表观组学十余年,领跑多组学科研服务的易基因。
2025年7月10日,徐州医科大学牛铭山教授和姚瑶教授团队合作,在国际血液学顶级期刊《Blood》(IF 23.1/Q1)上发表题为“Genetic and epigenetic mechanisms of GPRC5D loss after anti-GPRC5D CAR T-cell therapy in multiple myeloma”的重磅研究成果。此研究聚焦于多发性骨髓瘤(MM)患者接受靶向GPRC5D CAR-T细胞治疗后复发的耐药机制,利用整合全基因组测序(WGS)和全基因组甲基化测序(WGBS)技术,系统解析了GPRC5D抗原逃逸介导疾病复发的遗传学(双等位基因缺失,如纯合缺失)与表观遗传学(DNA高甲基化)双重机制,并通过靶基因DNA甲基化测序(Target-BS)技术在临床前模型中首次验证了去甲基化药物(阿扎胞苷)可逆转GPRC5D表观遗传沉默,为克服CAR-T耐药提供了精准干预新策略。深圳易基因为本研究提供DNA甲基化测序技术服务应用于CAR-T耐药机制研究,助力揭示DNA甲基化分析在肿瘤免疫治疗研究中的关键作用。

标题:Genetic and epigenetic mechanisms of GPRC5D loss after anti-GPRC5D CAR T-cell therapy in multiple myeloma(多发性骨髓瘤抗GPRC5D CAR-T细胞治疗后GPRC5D逃逸的遗传学和表观遗传学机制)
发表时间:2025-7-10
发表期刊:Blood
影响因子:IF23.1/Q1
技术平台:WGS、WGBS、Target-BS(易基因金牌技术)
作者单位:徐州医科大学、天津科技大学、美国哈佛医学院
DOI:10.1182/blood.2024026622

研究纳入10例抗GPRC5D CAR-T治疗后复发MM患者,对其复发期骨髓瘤细胞样本进行WGS和WGBS联合分析,发现80%病人出现GPRC5D抗原逃逸(丢失)或表达显著降低。其中3例存在显著GPRC5D双等位基因失活(纯合缺失或调控区域双等位缺失),而其余7例无基因突变的患者中,5例检出GPRC5D转录调控区域多位点高甲基化。此外,体外实验证实,多发性骨髓瘤细胞系的GPRC5D表达水平与其调控区域的甲基化水平呈显著负相关,而阿扎胞苷干预可显著恢复高甲基化细胞系(KMS11、IM9、RPMI-8226)的GPRC5D mRNA和蛋白表达。本研究不仅揭示了GPRC5D 逃逸和CAR-T治疗耐药的核心机制,更阐明了DNA甲基化动态监测在预测复发和干预中的关键价值。
- 抗原阴性逃逸是多发性骨髓瘤患者接受抗GPRC5D CAR-T细胞治疗后复发的关键驱动因子。
- GPRC5D纯合缺失和高甲基化是靶向抗原逃逸的重要机制。
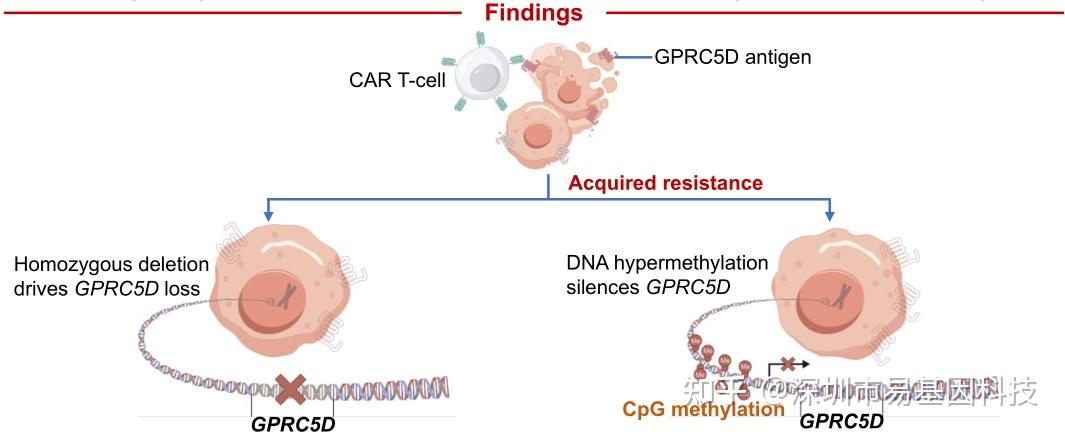
研究摘要
易基因相关拓展性产品案例
- 项目文章|多组学分析揭示坏死性小肠结肠炎(NEC)的新型DNA甲基化调控生物标志物及发病机制
- 项目文章|中山大学凌文华团队DNA甲基化研究揭示血管衰老与动脉粥样硬化的表观调控机制
- 项目文章|Sci Adv:WGBS+ChIP-seq揭示DNA甲基化在异基因造血干细胞移植后延迟血小板恢复中的关键作用
- 项目文章|WGBS揭示Vpr蛋白在HIV-1感染中对CD4+ T细胞DNA甲基化变化的作用
研究方法
患者样本:纳入10例接受抗GPRC5D CAR-T治疗后复发的MM患者,收集其复发期骨髓瘤细胞(CD138+)及配对正常细胞。
全基因组测序:对复发期CD138+ MM细胞及配对正常细胞进行WGS,检测拷贝数变异(CNV)、结构变异(SV)及单核苷酸变异(SNV),重点筛查GPRC5D位点的基因突变。
全基因组甲基化测序:分析全基因组甲基化水平差异,比较复发组MM细胞、未接受GPRC5D治疗的对照MM细胞及正常浆细胞的甲基化图谱,鉴定差异甲基化区域(DMRs)和差异甲基化位点(DMLs),筛选候选基因GPRC5D转录调控元件(启动子、增强子及基因间区)的CpG甲基化水平。
靶基因甲基化测序:靶向GPRC5D调控区域设计靶向捕获探针,在7种MM细胞系(KMS11、IM9、JJN3、RPMI-8226、KMS12-PE、NCI-H929、MM1S)中进行Target-BS高深度甲基化检测,验证特定CpG位点的甲基化状态和关键差异位点,并建立甲基化水平与基因表达的定量关联模型。
实验验证:
- qPCR:验证WGS检出的GPRC5D和TNFRSF17缺失断点;检测GPRC5D mRNA表达。
- 流式细胞术:GPRC5D抗体和BCMA抗体检测抗原阳性率,评估CAR-T治疗后抗原表达动态变化。
- 免疫组织化学(IHC):抗GPRC5D抗体和抗CD138抗体进行染色评估蛋白表达缺失。
- 药物干预实验:用1或3μM阿扎胞苷处理高甲基化MM细胞系,评估GPRC5D表达恢复情况。
结果图形
(1)接受抗GPRC5D CAR-T治疗后复发患者的临床特征
本研究纳入的10例MM复发患者中,中位年龄57.5岁(44-66岁),性别分布均衡。值得注意的是,90%患者存在高危细胞基因突变,80%为R-ISS II/III期,且既往接受过多线治疗(中位3.5线),提示该队列代表了临床上难治程度较高的MM人群。4例患者曾接受自体造血干细胞移植,1例患者(P10)在接受抗GPRC5D CAR-T前已接受抗BCMA CAR-T序贯治疗并进展为浆细胞白血病伴髓外病变(EMD)。CAR-T治疗后,所有患者均达到完全缓解(CR)或更好疗效,中位达最佳缓解时间为2.5个月,但中位无进展生存期(PFS)仅15.9个月(3-26.5个月),凸显复发问题的严峻性。免疫学监测显示,8例患者复发时GPRC5D表达完全阴性,2例呈GPRC5D+/-混合表达但以阴性细胞为主,提示抗原阴性逃逸是抗GPRC5D CAR-T治疗后复发的主导模式。这一特征显著区别于抗BCMA CAR-T治疗后常见的抗原阳性复发模式,为后续机制探索指明了方向。
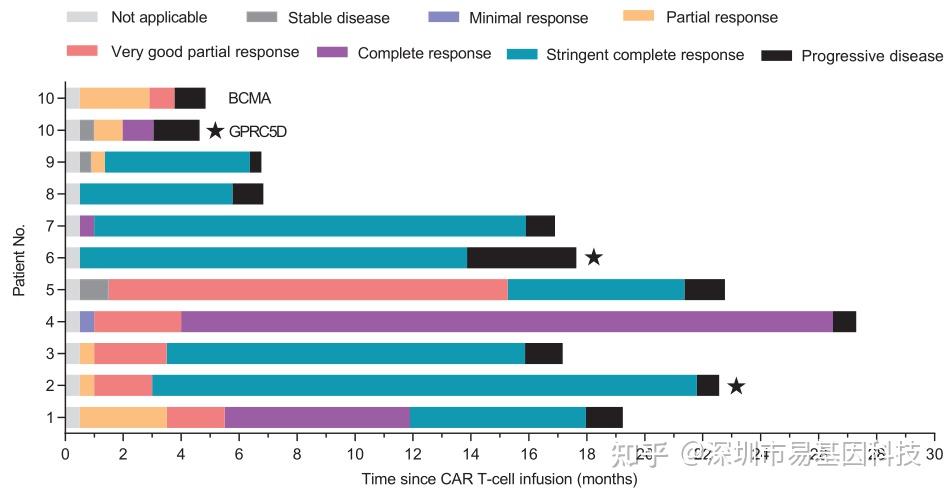
图1:分别靶向GPRC5D或BCMA CAR-T细胞治疗的临床疗效
(2)抗GPRC5D CAR-T治疗后GPRC5D基因的双等位缺失
患者1为女性MM复发患者,在接受抗GPRC5D CAR-T治疗后18个月复发,骨髓浆细胞浸润达24%。WGS分析揭示其染色体12p区域存在264 kb杂合缺失和22 kb纯合缺失,完全覆盖GPRC5D基因编码区,导致双等位基因失活。qPCR验证实验显示复发样本中同时检出杂合和纯合缺失拷贝(基线样本均阴性),证实该缺失为治疗后获得性克隆选择或治疗前极低频克隆扩增所致。IHC染色显示,GPRC5D在基线高表达,复发后完全缺失,而CD138表达保持稳定,验证其抗原逃逸的特异性。此案例首次在GPRC5D CAR-T背景下证实纯合缺失是抗原逃逸的主要机制,与BCMA CAR-T耐药机制高度相似,提示不同靶点CAR-T治疗面临共同的基因突变逃逸风险。
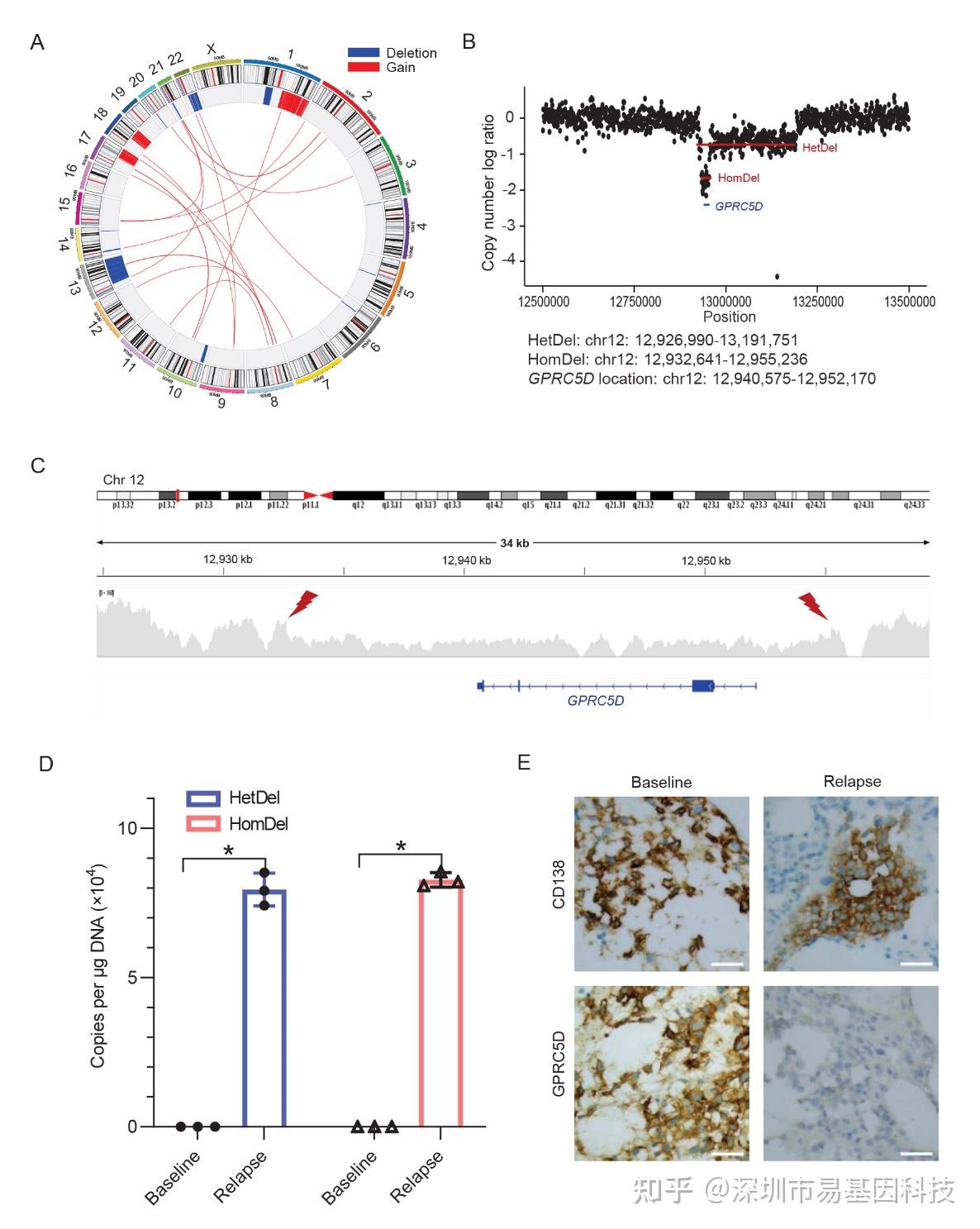
图2:抗GPRC5D CAR-T细胞治疗后患者1的GPRC5D基因双等位缺失
(3)CAR-T治疗后GPRC5D调控区域的纯合缺失
患者6为复杂性核型κ轻链MM,GPRC5D CAR-T治疗后13.9个月复发并进展为浆细胞白血病。WGS测序分析揭示其12号染色体上三个缺失片段:13.1 Mb杂合缺失、12.7 Mb杂合缺失和68.2 kb纯合缺失。qPCR证实缺失断点仅见于复发样本,且纯合缺失覆盖GPRC5D启动子及增强子区域,导致转录彻底沉默。RNA-seq未检出缺失exon1的替代转录本,证实该缺失的功能破坏性。IHC显示复发样本中GPRC5D阴性细胞占主导,但仍有36.7%细胞保留GPRC5D表达,与qPCR评估的亚克隆比例高度吻合。表明调控区域缺失可通过破坏转录启动导致抗原免疫逃逸,仅需小片段双等位缺失即可实现抗原沉默,且可与其他亚克隆的杂合缺失共存,形成复杂的克隆异质性图谱。该机制在CAR-T领域属首次系统证实。
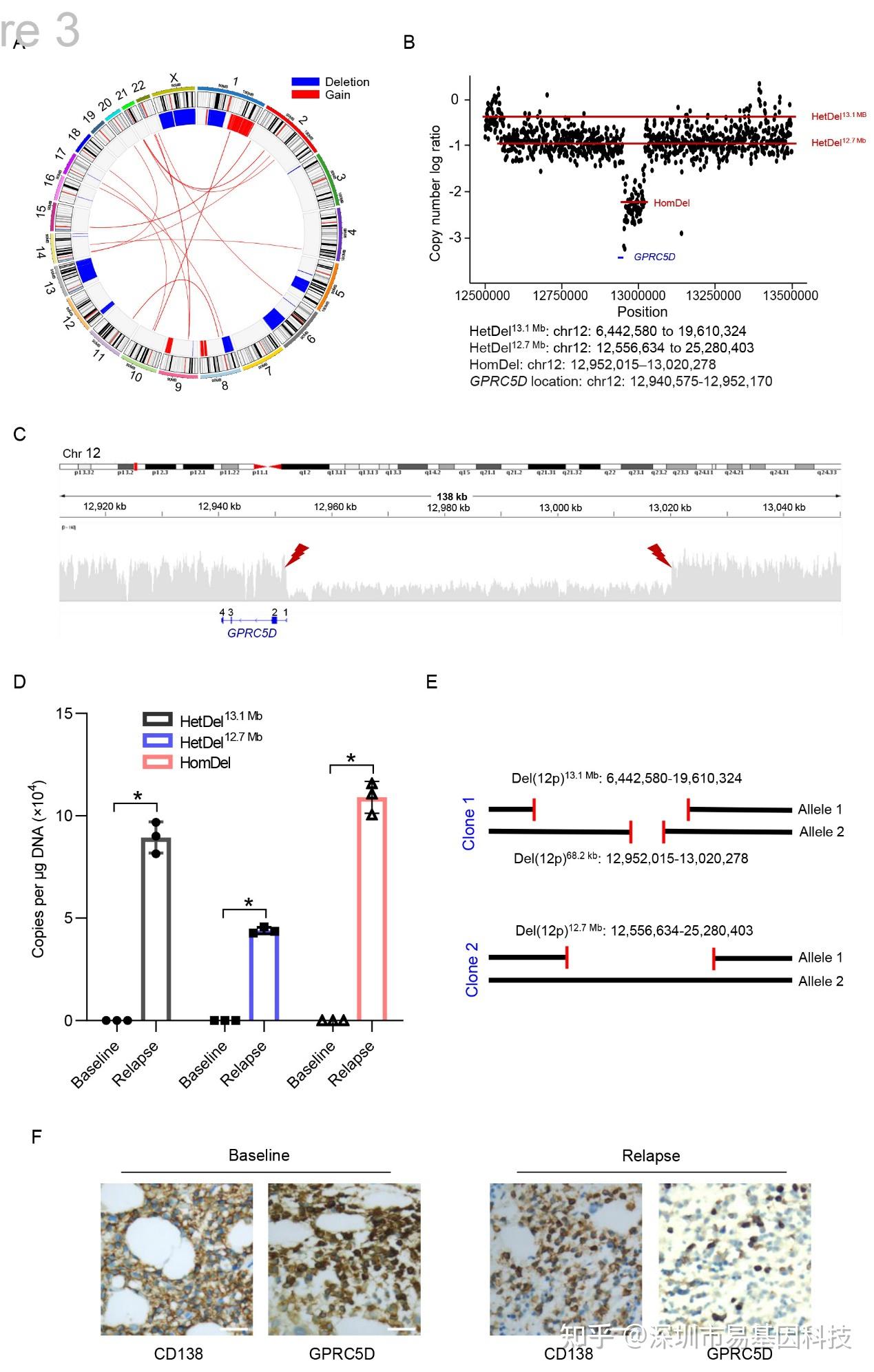
图3:CAR-T细胞治疗后患者6的GPRC5D调控元件纯合缺失
(4)CAR免疫风险导致BCMA与GPRC5D双重丢失
患者10序贯接受抗BCMA CAR-T(4个月后复发)和抗GPRC5D CAR-T治疗(3个月后再次复发),该IgG-κ型MM女性经7线治疗后进展为浆细胞白血病伴腹部EMD。复发样本的WGS分析揭示16号染色体存在1.02 Mb杂合缺失和5个局灶性纯合缺失,导致TNFRSF17(BCMA编码基因)双等位失活;12号染色体则存在13.3 Mb杂合缺失和3个局灶性纯合缺失,导致GPRC5D双等位失活。qPCR验证至少5个TNFRSF17和3个GPRC5D纯合缺失断点,提示基因组不稳定性驱动下多克隆并行演化。该患者经多线治疗后演变为至少15条染色体的复杂核型,证实患者基因组不稳定性容易介导多靶点抗原丢失。流式与IHC实验结果显示,治疗前BCMA与GPRC5D双高表达,复发后双抗原均阴性,导致CAR-T策略失效。此案例分析结果表明,对于基因组不稳定的高危患者,单靶点序贯治疗可能加速多抗原逃逸,多靶点CAR-T(如BCMA/GPRC5D双特异CAR)或联合去甲基化干预可能是更优选择。
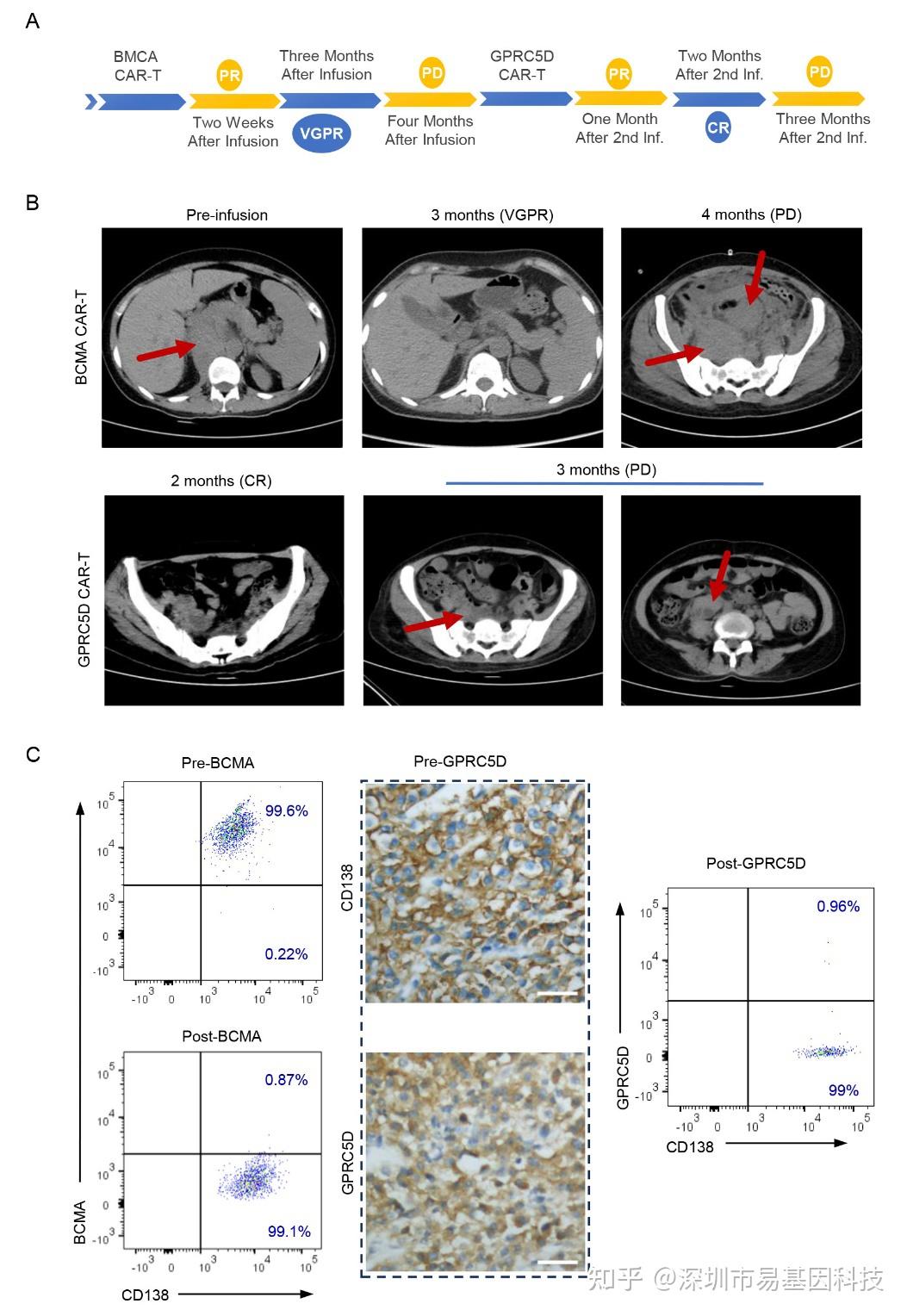
图4:患者10接受序贯抗BCMA和抗GPRC5D CAR-T细胞治疗后BCMA与GPRC5D双重丢失
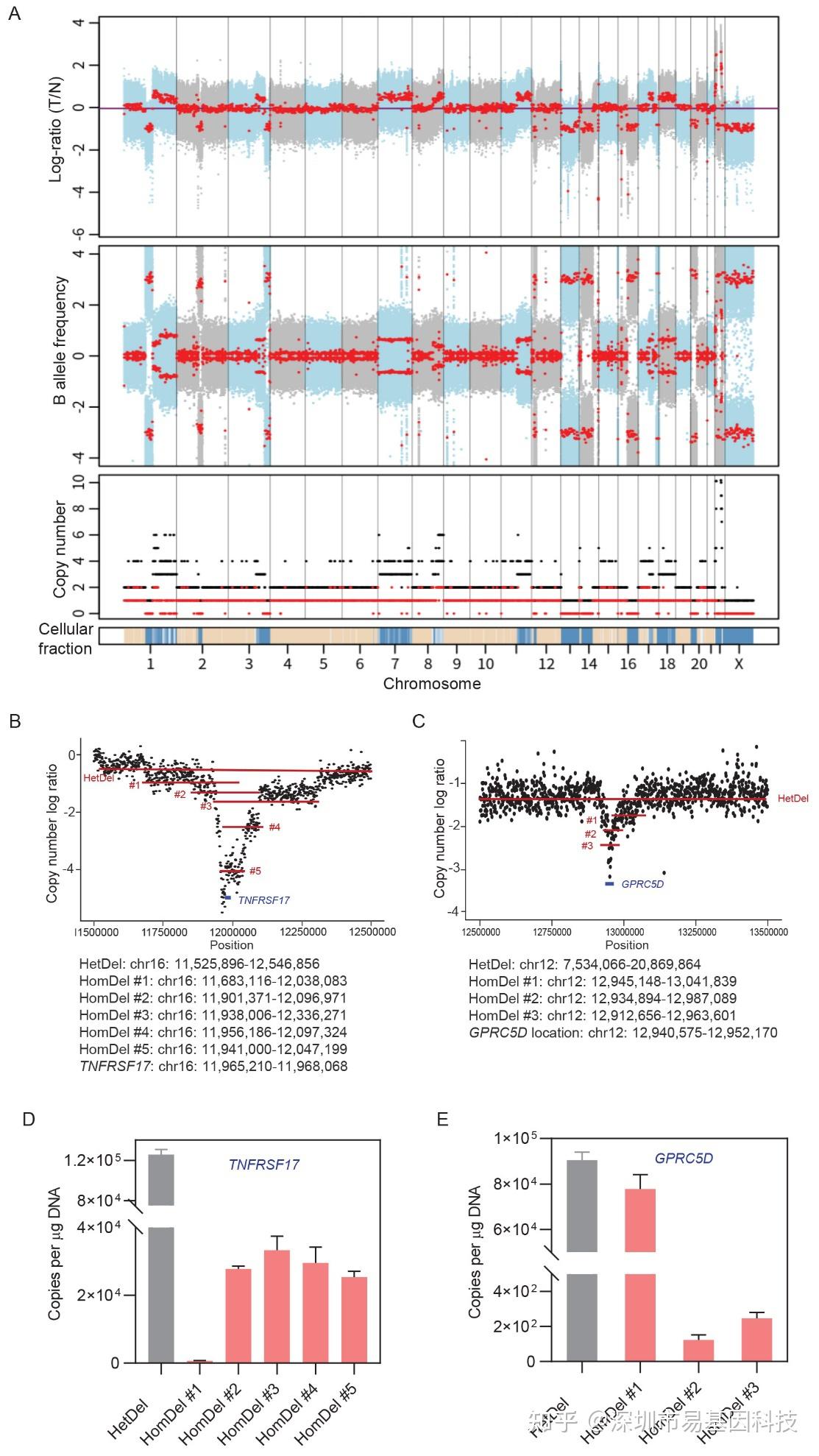
图5:全基因组测序(WGS)揭示BCMA和GPRC5D双重丢失的基因组学机制
(5)CAR-T治疗后复发MM细胞中GPRC5D的表观遗传沉默
在7例WGS未检出GPRC5D基因突变的复发患者中,WGBS分析结果显示5例MM复发患者存在GPRC5D调控区域高甲基化,靶向甲基化测序(Target-BS)分析结果显示多个CpG位点甲基化水平与GPRC5D表达负相关,揭示表观遗传重编程是主要逃逸机制。具体而言,复发MM细胞的全基因组甲基化水平相较于正常浆细胞呈显著低甲基化(MM特征),但相较于未接受GPRC5D治疗的对照MM细胞则表现为高甲基化,WGBS共鉴定出735.8万高甲基化DMLs和72万高甲基化DMRs,提示CAR-T治疗诱导特异性甲基化重编程。靶向GPRC5D位点的Target-BS测序分析揭示,5例复发患者在转录调控元件(启动子、增强子及内含子-外显子边界)呈现多位点高甲基化,而7例对照MM样本该区域均维持低甲基化状态。值得注意的是,两例正常浆细胞对照(GPRC5D阳性率仅10.1%和12.9%)也在该区域显示高甲基化,提示GPRC5D甲基化水平与表达呈负相关。
细胞系实验中,阿扎胞苷处理可诱导高甲基化细胞系(如RPMI-8226)的GPRC5D mRNA和蛋白表达上调,证明DNA高甲基化是独立的抗原沉默机制。
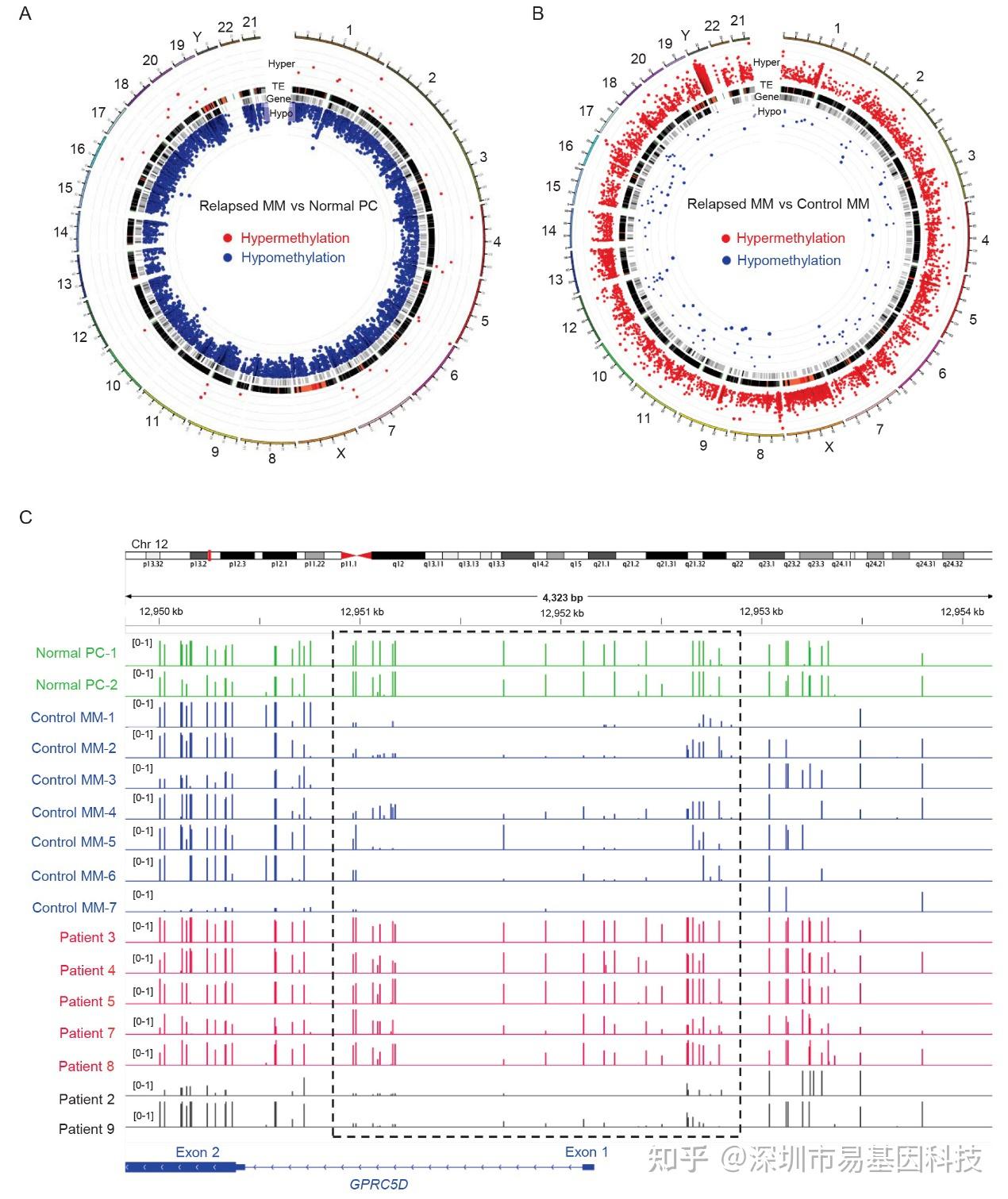
图6:GPRC5D CAR-T细胞治疗后多发性骨髓瘤细胞中GPRC5D位点的DNA高甲基化。
(A-B) 复发MM组与正常浆细胞(A)及对照MM组(B)相比,低甲基化或高甲基化差异甲基化区域(DMRs)的圈图。图中突出显示前10,000个DMRs。圈位置表示甲基化差异的显著性,红色圆圈代表高甲基化DMRs,其位置越靠外表示显著性越高;蓝色圆圈代表低甲基化DMRs,其位置越靠内表示显著性越高。
(C) IGV展示GPRC5D位点的DNA甲基化图谱。
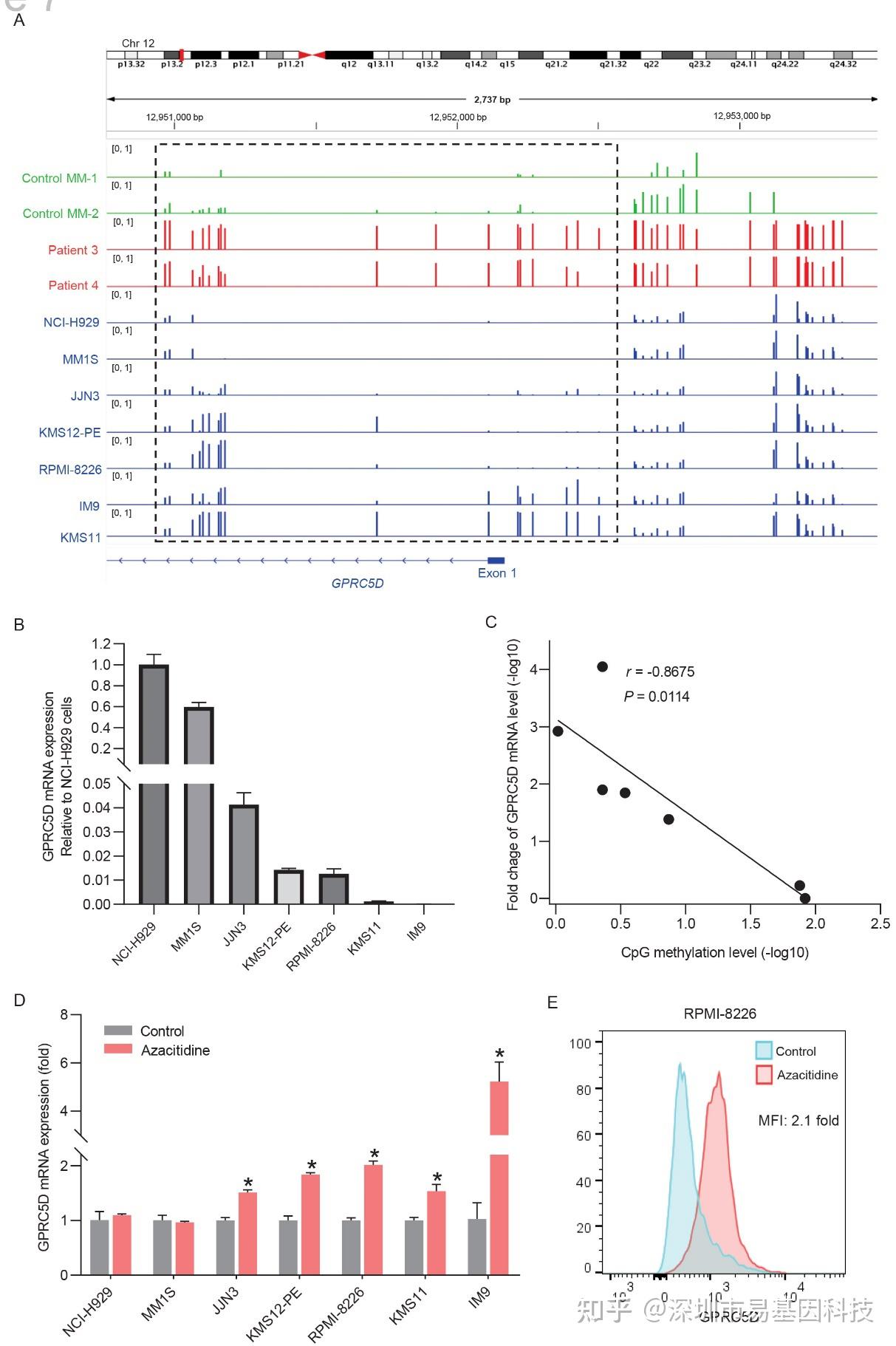
图7:多发性骨髓瘤细胞系中GPRC5D表达与甲基化水平的相关性。
- 7种多发性骨髓瘤细胞系GPRC5D基因调控区域靶基因甲基化Target-BS分析。IGV可视化展示CpG位点的甲基化信号。
- 多发性骨髓瘤细胞系中GPRC5D mRNA表达的qPCR分析。
- GPRC5D mRNA水平倍数变化与其调控区差异甲基化CpG位点平均甲基化水平之间的相关性分析。
- 阿扎胞苷处理诱导GPRC5D mRNA表达增加。
- 流式细胞术检测显示,RPMI-8226细胞经72小时阿扎胞苷处理后GPRC5D蛋白表达升高。
结论和启示
本研究证实GPRC5D免疫逃逸是CAR-T耐药的主要机制,且存在表观遗传沉默与遗传缺失。研究者发现去甲基化药物在细胞系中可部分逆转沉默,但临床转化需进一步优化给药策略。总之,靶向GPRC5D的联合疗法(如CAR-T+去甲基化药物)可能是克服耐药的新方向,未来研究需动态监测甲基化水平,实现耐药克隆的早期干预。
易基因的TBS技术是本研究从发现到验证的关键工具。TBS通过靶向捕获实现了:
超高深度:在GPRC5D调控区达到500×以上测序深度,精确检测单个CpG位点甲基化水平,分辨低丰度耐药亚克隆(<5%)。
成本效益:适合大规模样本队列(如本研究7个细胞系+多例临床样本)的快速验证,为WGBS发现的重要DMRs提供经济可行的临床转化路径。
功能关联:TBS数据与qPCR表达数据精准配对,建立甲基化-表达回归模型,筛选出调控效能最强的CpG位点,为后续开发甲基化特异性引物用于MRD监测提供靶点。
易基因DNA甲基化整体研究方案
DNA甲基化是一种表观遗传修饰,指DNA分子在DNA甲基转移酶的作用下将甲基选择性地添加到特定碱基上的过程。主要发生在胞嘧啶的CpG位点,也可以在非CpG位点和CpG岛中发生。DNA甲基化参与调控基因表达、X染色体失活、基因印记、胚胎发育、细胞分化、肿瘤发生以及维持基因组稳定性。
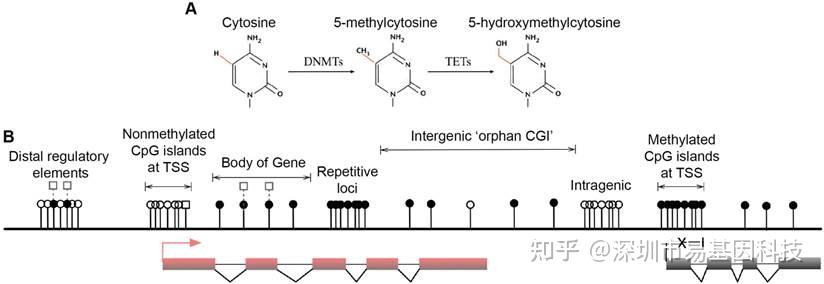
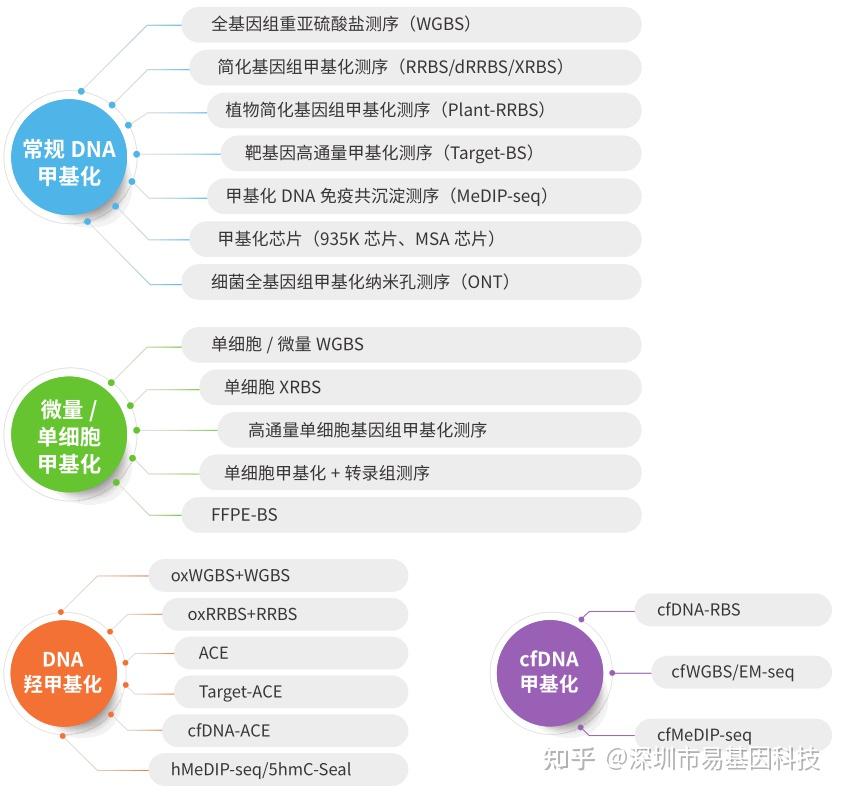
易基因DNA甲基化研究技术优势
参考文献:
Ma S, Xia J, Zhang M, Li W, Xiao M, Sha Y, Wang W, Zhou J, Wang Y, Qi K, Fu C, Sun Z, Zhou D, Sun Q, Qiu T, Yan Z, Zhu F, Chen W, Cheng H, Sang W, Cao J, Li D, Li ZZ, Fulciniti M, Yao Y, Xu K, Niu M. Genetic and epigenetic mechanisms of GPRC5D loss after anti-GPRC5D CAR T-cell therapy in multiple myeloma. Blood. 2025 Mar 16. doi: 10.1182/blood.2024026622.
相关阅读:
1.2024项目文章精选:DNA甲基化、RNA甲基化(m6A/m5C)、ChIP-seq、单细胞转录组、宏基因组|年终盘点
2.项目文章|多组学分析揭示坏死性小肠结肠炎(NEC)的新型DNA甲基化调控生物标志物及发病机制
3.项目文章|中山大学凌文华团队DNA甲基化研究揭示血管衰老与动脉粥样硬化的表观调控机制
4.项目文章|Sci Adv:WGBS+ChIP-seq揭示DNA甲基化在异基因造血干细胞移植后延迟血小板恢复中的关键作用
5.项目文章|WGBS揭示Vpr蛋白在HIV-1感染中对CD4+ T细胞DNA甲基化变化的作用


 浙公网安备 33010602011771号
浙公网安备 33010602011771号