9.19
今天你好像让 cxl 给你讲为什么 \(\text{CO}\) 不会和酸碱反应来着。不知道她给你讲了没有。
如果你不想看这一长串文字,可以直接跳到最后。
氧化物可以大致分为 成盐氧化物 和 不成盐氧化物。
其中 成盐氧化物 又大致分为 酸性氧化物,碱性氧化物,两性氧化物。
成盐氧化物
酸性氧化物
酸性氧化物 就是与碱反应生成 对应盐 和水的氧化物。非金属氧化物 大多 是酸性氧化物,比如 \(\text{CO}_2,\text{SO}_2,\text{SO}_3\)。
\[\require{mhchem}
\require{autoload-all}
\require{mediawiki-texvc}\begin{split}{\color{green}\text{CO}_2}+2\text{NaOH}\xlongequal{\quad}{\color{green}{\text{Na}_2\text{CO}_3}}+\text{H}_2\text{O}\\{\color{green}\text{SO}_2}+2\text{NaOH}\xlongequal{\quad}{\color{green}{\text{Na}_2\text{SO}_3}}+\text{H}_2\text{O}\\{\color{green}\text{SO}_3}+2\text{NaOH}\xlongequal{\quad}{\color{green}{\text{Na}_2\text{SO}_4}}+\text{H}_2\text{O}\end{split}\]
为什么我要强调 对应盐 呢?因为 \(\text{NO}\) 这个东西也会和 \(\text{NaOH}\) 反应。
长这样
\[\mathop{\text{N}}\limits^{+2} \text{O}+\text{NaOH}\xlongequal{\quad}\text{N}_2\text{O}+\text{H}_2\text O+{\color{red}\text{Na}\mathop{\text{N}}\limits^{+3}\text{O}_2}
\]
这里 \(\text{NaNO}_2\) 也是盐,但是这里的 \(\text N\) 化合价为 \(+3\),和 \(\text{NO}\) 中的 \(+2\) 不对应,所以 \(\text{NO}\) 不能算作酸性氧化物。
碱性氧化物
碱性氧化物 类似,就是与酸反应生成对应盐和水的氧化物。碱性氧化物 一定 是金属氧化物。
反之则不然。比如 \(\text{Mn}_2\text{O}_7\) 是酸性氧化物。因为
\[\text{Mn}_2\text{O}_7+2\text{NaOH}\xlongequal{\quad} 2\text{NaMnO}_4+\text{H}_2\text O
\]
两性氧化物
而 \(\text{Al}_2\text{O}_3\) 则是 两性氧化物。顾名思义,就是又体现酸性又体现碱性。
\[\begin{cases}\text{Al}_2\text{O}_3+2\text{NaOH}\xlongequal{\quad}2\text{NaAlO}_2+\text{H}_2\text{O}\\\text{Al}_2\text O_3+6\text{HCl}\xlongequal{\quad}2\text{AlCl}_3+3\text{H}_2\text O\end{cases}
\]
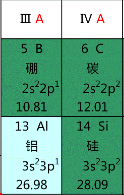
我们可以从元素周期表上看出一点端倪。因为铝处于金属与非金属的交界处,所以它显现出这种矛盾的性质因该是可以理解的()
不成盐氧化物
这就是解释了你最开始的那个疑问,因为 \(\text{CO}\) 属于不成盐氧化物,所以它既不会与酸反应,也不会与碱反应。
其他的不成盐氧化物还有我们开头提到的 \(\text{NO}\) 以及常见的催化剂 \(\text{MnO}_2\)。
\[\begin{cases}\mathop{\text{Mn}}\limits^{+4}\text{O}_2+4\text{HCl(浓)}\xlongequal{\ \Delta\ }{\color{red}\mathop{\text{Mn}}\limits^{+2}}\text{Cl}_2+\text{Cl}_2\uparrow+2\text{H}_2\text O\\\text{和碱的有点复杂,我不太会()}\end{cases}
\]
但是这话说了跟没说好像没有什么区别。除了根据氧化物的这个是否与酸碱反应来判断是否成盐外,我们能不能用其他的方法,先判断出它是否成盐,然后再得知它是否会与酸碱反应呢?
有的!
酸酐
酸酐(顾名思义)就是把这个酸中的 \(\text{H}_2\text O\) 给脱掉(干)。
举些例子
\[\begin{aligned}\text{H}_2\text{SO}_4&\to\text{SO}_3\\\text{H}_2\text{CO}_3&\to\text{CO}_2\\\text{HNO3}&\to\text{N}_2\text{O}_5&\color{green}\text{因为是按 H}_2\text{O 氢与氧二比一脱去的(有点类似浓硫酸的脱水性)}\end{aligned}
\]
碱性氧化物都是金属氧化物也不太会考,就记住上面 \(\text{Al}_2\text{O}_3\) 是两性氧化物和 \(\text{Mn}_2\text{O}_7\) 是酸性氧化物 \(\text{MnO}_2\) 是不成盐氧化物的特例就行。
比较麻烦的是酸性氧化物。
其规律是,所有是酸酐的氧化物,都是酸性氧化物。
比方说
\[\begin{aligned}\text{Mn}_2\text{O}_7&\gets \text{HMnO}_4&\color{green}\text{高锰酸}\end{aligned}
\]
这个 \(\text{CO}\) 显然不存在一种酸是 \(\text{H}_2\text{CO}_2\)。当然有个有机酸叫甲酸或者叫蚁酸 \(\text{HCOOH}\),不过这两个完全不是一个东西 \(\text{HCOOH}\xlongequal{\quad}\text{H}^++\text{COOH}^{-}\)。
很好,就是这样。打了 1 个 h 字,顺便复习了一下杜岳暑假里讲的一点点东西,希望你可以看懂一点点()
生日快乐!!!




 浙公网安备 33010602011771号
浙公网安备 33010602011771号